| A.水;无水CaCl2固体 | B.饱和NaHCO3溶液;浓H2SO4 |
| C.浓H2SO4;饱和NaHCO3溶液 | D.饱和NaHCO3溶液;稀H2SO4 |
下列图象能正确地表达可逆反应3A(g)+B(g)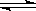 2C(g)(△H<0)的是( )
2C(g)(△H<0)的是( )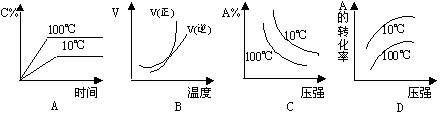
在下列给定条件的溶液中,一定能大量共存的离子组是 ( )
| A.无色溶液:Ca2+、H+、Cl-、HSO | B.能使甲基橙呈红色的溶液:Na+、NH、I-、NO |
| C.NaOH溶液:K+、Fe3+、SO、NO | D.=0.1 mol/L的溶液:Na+、K+、SiO、NO |
用蒸馏水稀释0.1 mol/L醋酸时,始终保持增大趋势的是 ( )
| A.溶液中的c(CH3COO-) | B.溶液中的c(H+) |
| C.醋酸的电离平衡常数 | D.溶液中的c(OH-) |
某合金(仅含铜和铁)中铜和铁的物质的量之和为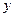 mol,其中Cu的物质的量分数为
mol,其中Cu的物质的量分数为 ,将其全部投入50 mL
,将其全部投入50 mL 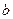 mol/L的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物),下列说法正确的是()
mol/L的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物),下列说法正确的是()
①若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
②若金属全部溶解,则溶液中一定含有Fe3+
③若金属全部溶解,且产生336 mL气体(标准状况),则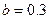
④当溶液中金属离子只有Fe3+、Cu2+时,则 与
与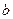 的关系为:
的关系为: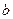 ≥80
≥80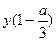
| A.①② | B.②③ | C.③④ | D.①④ |
把一块镁铝合金投入到1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法中正确的是()
| A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中 |
| B.b值越大,合金中Mg的含量越高 |
| C.c值越大,合金中Al的含量越高 |
| D.假设a=25,整个反应过程中,主要发生了5个离子反应 |