设C+CO2 2CO-Q1,反应速率为v1;N2+3H2
2CO-Q1,反应速率为v1;N2+3H2 2NH3+Q2,反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为
2NH3+Q2,反应速率为v2,对于上述反应,当温度升高时,v1和v2的变化情况为
| A.同时增大 | B.同时减小 |
| C.v1增大,v2减小 | D.v1减小,v2增大 |
下图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是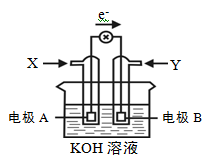
| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是 
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2+ + 2e- = Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,Cu2+向铜电极移动 |
已知合成氨反应N2(g)+3H2(g) 2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:
2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据: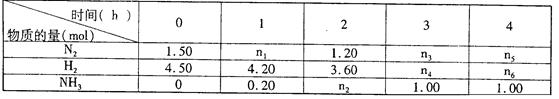
下列说法正确的是
| A.反应进行到1小时时放出的热量为9.23kJ |
| B.反应3h内,反应速率v(N2)为0.17mol·L-1·h-1 |
| C.此温度下,该反应的平衡常数为0.037 |
| D.4h时,若再加入1mol N2,达到新的平衡时,N2的转化率是原来的两倍 |
在密闭容器中进行下列反应:M(g)+N(g)===R(g)+2L。此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是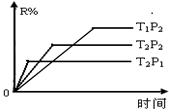
| A.正反应为吸热反应 L是气体 |
| B.正反应为放热反应 L是气体 |
| C.正反应为吸热反应 L是固体 |
| D.正反应为放热反应 L是固体或液体 |
在密闭容器中充入一定量的NO2,发生反应2NO2(g) 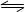 N2O4(g)△H=﹣57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g)△H=﹣57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是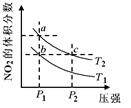
| A.a、c两点的反应速率:a>c |
| B.a、b两点的转化率:a<b |
| C.a、c两点气体的颜色:a深,c浅 |
| D.由a点到b点,可以用加热的方法 |