相同容积的四个密闭容器中进行同样的可逆反应:
2A(g)+B(g)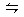 3C(g)+2D(g)
3C(g)+2D(g)
起始时四个容器所盛A、B的物质的量分别为
| |
甲 |
乙 |
丙 |
丁 |
| A/mol |
2 |
1 |
2 |
1 |
| B/mol |
1 |
1 |
2 |
2 |
在相同温度下建立平衡时,A或B的转化率大小关系正确的是( )。
A.αA:甲<丙<乙<丁 B.αA:甲<乙<丙<丁
C.αB:甲<丙<乙<丁 D.αB:丁<乙<丙<甲
物质的量相同的下列溶液中,含粒子种类最多的是:
| A.HCl | B.NH4Cl | C.K2S | D.CH3COONa |
下列各离子方程式属于水解反应,且可使溶液呈酸性的是
A.HS-+H2O  H3O++S2- H3O++S2- |
B.NH4++2H2O NH3·H2O+H3O+ NH3·H2O+H3O+ |
C.HCO3-+OH- CO32-+ H2O CO32-+ H2O |
D.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
已知在等温等压条件下,化学反应方向的判据为:
△H-T△S<0反应能正向自发进行
△H-T△S=0反应达到平衡状态
△H-T△S>0反应不能自发进行
设反应A(s)  C(g) +D(g)△H-T△S="(-4500+11T)" J/mol,要防止反应发生,温度必须:
C(g) +D(g)△H-T△S="(-4500+11T)" J/mol,要防止反应发生,温度必须:
| A.高于409K | B.低于136 K |
| C.高于136K而低于409K | D.低于409K |
氯气溶于水达到平衡形成饱和溶液,若其他条件不变,只改变某一条件,下列叙述正确的是:
| A.再通入少量氯气,c(H+)/ c(ClO-)减小 |
| B.通入具有漂白性的SO2气体,溶液的漂白性增强 |
| C.氯水中存在的分子、离子共5种 |
| D.加入少量水,水的电离平衡向正反应方向移动 |
若溶液中由水电离产生的c(OH-)= 1×10-14mol·L-1,向该溶液中加入下列各组离子可以大量共存的是:
| A.K+、Na+、Cl-、AlO2— | B.Ba 2+、Na+、Cl-、HCO3— |
| C.K+、Fe3+、SO42—、CO32— | D.Na+、NH4+、C1-、OH— |