下列说法中正确的是
A.聚合硫酸铁可用于净水,其化学式为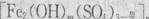 ,式中的m可能为6 ,式中的m可能为6 |
| B.将3g白色粉未完全溶于10g热水中冷却至室温析出2g晶体,再将析出的2g晶体全部溶于10 g热水中,冷却至室温析出1.5 g晶体。由此可知此白色粉末可能是纯净物也可能是混合物 |
| C.无色混合气体甲依次经过下图所示实验装置的处理,结果得到酸性溶液且最终无气体剩余.则原气体的成分可能为NH3、NO、CO2 |
| D.淀粉和纤维素的组成都是(C6H10O5)n,水解的最终产物都是葡萄糖,蛋白质是由氨基酸形成的可降解的高分子化合物 |