草酸是二元中强酸,测得0.01 mol·L-1的草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L-1 NaHC2O4溶液中滴加0.01 mol·L-1 NaOH溶液,随着NaOH溶液体积的增加,下列说法正确的是
| A.V(NaOH) = 0时, c(Na+)> c(H+)> c(HC2O4- )> c(C2O42-)> c(OH-) |
| B.V(NaOH) = 5时, c(Na+)=c(C2O42-)+c(HC2O4- )+c(H2C2O4) |
| C.V(NaOH) =" 10" mL时, c(Na+) = c(HC2O4- )+2c(C2O42-) |
| D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4- ) |
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是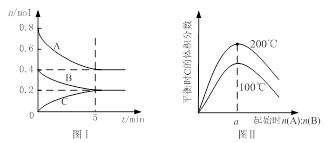
A.200℃时,反应从开始到平衡的平均速率v(B)=" 0." 02 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于0.5
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)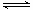 SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是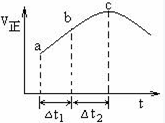
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.△t1=△t2时,SO2的转化率:a~b段小于b~c段 |
如图所示,是在其他条件一定时,反应2A+B 2C△H<0,A的最大转化率与温度关系曲线,下列叙述正确的是
2C△H<0,A的最大转化率与温度关系曲线,下列叙述正确的是
| A.X或Y两点相应,V(正)>V(逆) |
| B.Z、N两点表示未达平衡状态,且都是V(正)>V(逆) |
| C.W点表示非平衡状态,V(正)>V(逆) |
| D.相应反应速率大小的点:W > Y > N |
下图是关于反应A2(g)+3B2(g)===2C(g) △H<0的平衡移动图形,影响平衡移动的原因是
| A.升高温度,同时加压。 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂; |
| D.增大反应物浓度,同时减小生成物浓度 |
已知4NH3(g)+5O2(g)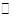 4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1是一个可逆反应。若反应物起始物质的量相同,则下图中关于该反应不正确的是
4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1是一个可逆反应。若反应物起始物质的量相同,则下图中关于该反应不正确的是 