镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应:Mg+2H++H2O2= Mg2++2H2O。关于该电池说法正确的是
| A.镁合金为电源负极,发生氧化反应 | B.放电时H+在正极反应得电子 |
| C.正极方程式为:H2O2+2e-=2OH- | D.放电时正极的pH降低 |
【改编】电化学方法是工业上常采用的一种污水处理方法。某含氮废水中含有NO3-,其降解的原理如图所示: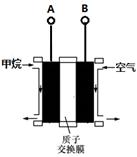
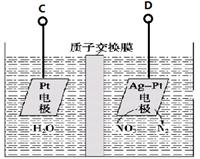
下列说法中不正确的是
| A.燃料电池的A极连接电解池的D级 |
| B.A电极的电极反应式为:CH4-8e-+2H2O = CO2+8H+ |
| C.燃料电池工作时H+移向左边 |
| D.每消耗标况下5.6 L甲烷,则电解池交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g |
【改编】用下列实验装置进行相应实验,能达到实验目的的是
| A.用图1 所示装置除去鸡蛋清中含有的少量实验杂质 |
| B.用图2 所示装置蒸干MgCl2饱和溶液制备无水MgCl2晶体 |
| C.用图3 所示装置从海水制取蒸馏水 |
| D.用图4 所示装置分离酒精萃取碘水中的碘 |
【原创】下列离子方程式错误的是
| A.锅炉中可以用纯碱除水垢: CaSO4 + CO32-═ CaCO3+ SO42- |
| B.用KMnO4测定蔬菜中草酸含量:2MnO4-+5H2C2O4+6H+ =2Mn2+ +10CO2↑+8H2O |
| C.Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2↑+S↓+2H2O |
D.用铜电极电解饱和氯化钠溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
【原创】用NA表示阿伏加德罗常数,下列说法错误的是
| A.2g重水(2H2O)中含有的质子数为NA |
| B.1 mol NaHSO4在熔融时离子总数为3NA |
| C.常温常压下,等质量的CO2、N2O含有相同的分子数 |
| D.1molNa2O2与足量CO2充分反应转移的电子数目为NA |
【原创】化学与生产、生活、社会密切相关。下列有关说法中,错误的是
| A.新农村建设大量使用秸秆制取沼气,符合低碳理念 |
| B.卤水点豆腐、血液透析、静电除尘都是利用了胶体的性质 |
| C.洪水过后的水源很浑浊,可加入明矾净化和消毒 |
| D.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |