将三种气态烃以任意比例混合,与足量的氧气在密闭容器里完全燃烧,在温度不变的条件下(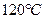 )其压强也不变,推断这三种烃的分子式________,由此可以总结出什么规律?
)其压强也不变,推断这三种烃的分子式________,由此可以总结出什么规律?
在恒温时,向某密闭容器中通入2 mol X和1 mol Y气体,发生如下反应:2X(g)+Y(g) 2Z(g),压强一定时,测得在平衡时Z的体积分数为0.4。
2Z(g),压强一定时,测得在平衡时Z的体积分数为0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4 mol X(g)和2 mol Y(g),达到平衡,则Z的体积分数为_______;平衡时,气体X的体积分数为_______。
(2)与上述平衡保持同温、同压,若向密闭容器中通入X(g)和Y(g)的物质的量分别记为n(X)=m、n(Y)=n,并满足平衡时Z的体积分数为0.4,则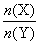 的取值范围为_______。
的取值范围为_______。
在一定条件下,将2 mol SO2和1 mol O2通入一个容积固定的密闭容器中,发生如下反应:2SO2+O2 2SO3,当此反应进行到一定程度时,反应混合物处于化学平衡状态。若维持容器温度不变,令a,b,c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如a,b,c取不同的值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同。请填写下列空白:
2SO3,当此反应进行到一定程度时,反应混合物处于化学平衡状态。若维持容器温度不变,令a,b,c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如a,b,c取不同的值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同。请填写下列空白:
(1)若a=0,b=0,则c=______;
(2)若a=0.5,则b=______,c=______;
(3)a,b,c必须满足的一般条件是(请用两个化学方程式表示,其中一个只含a和c,另一个只含b和c):__________________,________________________。
在密闭容器中进行的如下反应:2SO2(g)+O2(g)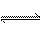 2SO3(g) ,SO2的起始浓度是0.4 mol·L-1,O2的起始浓度是1 mol·L-1。当SO2的转化率为80%时,反应达到平衡状态
2SO3(g) ,SO2的起始浓度是0.4 mol·L-1,O2的起始浓度是1 mol·L-1。当SO2的转化率为80%时,反应达到平衡状态
(1)求反应的平衡常数。
(2)若将平衡时反应混合物的压强增大1倍,平衡将如何移动?
(3)若平衡时反应混合物的压强减小1倍,平衡将如何移动?
(4)平衡时保持体积不变,向平衡混合气体中充入稀有气体Ar,使体系总压变为原来的3倍,平衡又将如何移动?
Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g) 4AC2(g)+B2(g),在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是_______(用含a的代数式表示);
4AC2(g)+B2(g),在上述条件下,向容器中充入AC和BC2各1 mol达平衡时,生成AC2和B2共a mol,则AC的转化率是_______(用含a的代数式表示);
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1 mol,达平衡时生成AC2和B2共b mol,将b与Ⅰ中的a进行比较,则a_______b (填“>”“<”“=”或“不能确定”)
现有中学常见的三种单质甲、乙、丙,它们在一定条件下能发生如下变化,其中次要生成物已略去。
(1)已知乙元素的+2价离子与Ne原子具有相同的电子层结构,则②的离子方程式为____
____________________,④的化学方程式为________________________。
(2)若反应①可在常温下进行,则A的名称是_____________。若反应①需在加热条件下进行,则A的名称是_____________,反应的化学方程式为_____________________________。
(3)从C溶液中得到C需经过两步操作:先从C溶液中得到晶体,再将得到的晶体转化为C。从C溶液中得到晶体的过程被称为________________________,将得到的晶体转化为C的实验条件是______________________________________。