NO的生物活性已引起科学家高度重视。它与超氧离子(O2— )反应,该反应的产物本题用A为代号。在生理pH值条件下,A的半衰期为1-2秒。A被认为是人生病,如炎症、中风、心脏病和风湿病等引起大量细胞和组织毁坏的原因。A在巨噬细胞里受控生成却是巨噬细胞能够杀死癌细胞和入侵的微生物的重要原因。科学家用生物拟态法探究了A的基本性质,如它与硝酸根的异构化反应等。他们发现,当16O标记的A在18O标记的水中异构化得到的硝酸根有11% 18O,可见该反应历程复杂。回答如下问题:(1)写出A的化学式。写出NO跟超氧离子的反应。这你认为A离子的可能结构是什么?试写出它的路易斯结构式(即用短横表示化学键和用小黑点表示未成键电子的结构式)。(2)A离子和水中的CO2迅速一对一地结合。试写出这种物种可能的路易斯结构式。(3)含Cu+离子的酶的活化中心,亚硝酸根转化为一氧化氮。写出Cu+和NO2–在水溶液中的反应。(4)在常温下把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50oC,发现气体的压力迅速下降,压力降至略小于原压力的2/3就不再改变,已知其中一种产物是N2O,写出化学方程式。并解释为什么最后的气体总压力略小于原压力的2/3。
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。
请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为;
(3)在溶积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);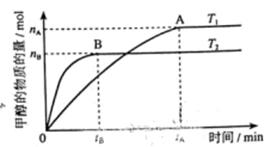
下列说法正确的是________(填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为:v(CH3OH)=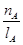 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时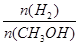 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______;
(8分)向甲乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同条件下(温度T ℃),发生下列反应:A(g)+B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
回答下列问题:
(1)乙容器中,平衡后物质B的转化率________;
(2)x=________;
(3)T ℃时该反应的平衡常数为________;
(4)下列说法正确的是________。
A.向平衡后的乙容器中充入氦气可使c(A)增大
B.将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同
C.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol-1
把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100 mL的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则
(1)两个电极均可收集到的气体在标准状况下的体积为L;
(2)电路中共转移mol电子;
(3)铝元素最终的存在形式为。
(6分)利用盖斯定律解答下列各小题
(1)已知反应:H2(g)+ O2(g)==H2O(g)△H1 N2(g)+2O2==2NO2(g)△H2
O2(g)==H2O(g)△H1 N2(g)+2O2==2NO2(g)△H2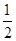 N2(g)+
N2(g)+ H2(g)==NH3(g)△H3
H2(g)==NH3(g)△H3
利用上述三个反应,计算4NH3(g)+7O2(g)==4NO2(g)+6H2O(g)的反应焓变为(用含△H1、△H2、△H3的式子表示)。
(2) 已知:CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g)ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:。
(本题共10分)白磷、红磷是磷的两种同素异构体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足是生成P4O10。
(1)已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)=P4O10(s) ΔH1=" -2983.2" kJ•mol-1,
P(s,红磷)+ 5/4O2(g)="1/4" P4O10(s) ΔH2=" -738.5" kJ•mol-1
则该温度下白磷转化为红磷的热化学方程式为。
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)=P4O6(s) ΔH= -1638kJ•mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况下),控制条件使之恰好完全反应。则所得到的P4O10和P4O6的物质的量之比为,反应过程中放出的热量为为。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下的化学键的键能(KJ/mol):P-P 198,Cl-Cl 243,P-Cl 331。
则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热ΔH =。