对于平衡体系mA(g)+nB(g) pC(g)+qD(g);△H<0 。下列结论中不正确的是
pC(g)+qD(g);△H<0 。下列结论中不正确的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B 的转化率相等,说明反应开始时,A、B的物质的量之比为 m : n
C.若温度不变时,压强增大到原来的2倍,达新平衡时,总体积一定比原来的1/2要小
D.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol
下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通 后,使c、d两点短路.
后,使c、d两点短路.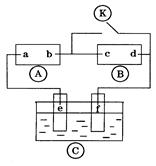
下列叙述正确的是
| A.a为直流电源的负极 |
| B.d极发生的反应为2H++2e-=H2↑ |
| C.f电极为铜板 |
| D.e极发生的反应为Cu-2e- =Cu2+ |
控制适合的条件,将反应2Fe3++2I-==2Fe2++I2,设计成如下图所示的原电池。下列判断不正确的是
| A.反应开始时,乙中石墨电极上发生氧化反应 |
| B.反应开始时,甲中石墨电极上Fe3+被还原 |
| C.电流计读数为零时,反应达到化学平衡状态 |
| D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
一定条件下,在密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2(g)+O2(g)  2SO3(g);△H=-akJ·mo1-1在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是
2SO3(g);△H=-akJ·mo1-1在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是
| A.4 mo1SO2和2mol O2 |
| B.4mol SO2、2mo1 O2和2mol SO3 |
| C.4mol SO2.和4 mo1 O2 |
| D.6mo1 SO2和4 mo1 O2 |
在恒温条件下,体积固定的密闭容器中,进行可逆反应A(s)+3B(g) 3C(g),下列不能说明可逆反应达到平衡状态的是
3C(g),下列不能说明可逆反应达到平衡状态的是
| A.B的浓度不再变化 |
| B.混合气体的压强不再变化 |
| C.混合气体的密度不再变化 |
| D.混合气体的平均相对分子质量不再改变 |