b g某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气。则该金属的相对原子质量为( )
A.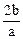 |
B. |
C. |
D.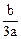 |
短周期元素W、X、Y和Z的原子序数依次增大。W原子是半径最小的原子,非金属元素X形成的一种单质能导电,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| B.元素X与W形成的共价化合物有很多种 |
| C.元素W、X的氯化物中,各原子均满足8电子的稳定结构 |
| D.元素Z可与元素X形成共价化合物XZ2 |
在一定温度下,向2L密闭容器中加入1mol X和2mol Y,发生如下反应:
X(g)+2Y(g) 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
| A.容器内气体混合物的密度不随时间变化 |
| B.容器内X、Y、Z的浓度之比为1∶2∶2 |
| C.单位时间内消耗0.1mol X,同时生成0.2mol Y |
| D.单位时间内消耗0.1mol X,同时生成0.2mol Z |
下列说法中正确的有的是
| A.决定化学反应速率的主要因素是参加反应的物质的性质 |
| B.催化剂可以使不起反应的物质发生反应 |
| C.可以找到一种催化剂使水变成汽油 |
| D.催化剂是决定化学反应速率的主要因素 |
下图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是
①X的气态氢化物与Y最高价氧化物对应的水化物的溶液能发生反应生成盐
②同浓度的Y、Z的气态氢化物的水溶液的酸性Y< Z
③Z的单质常温下是深红棕色液体,具有氧化性
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
| A.只有③ | B.只有①④ |
| C.只有①②③④ | D.①②③④⑤ |
已知一定温度时:N2(g)+3 H2(g) 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入1mol N2和3mol H2,达到平衡时放出热量为Q。则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入1mol N2和3mol H2,达到平衡时放出热量为Q。则下列关系式中正确的是
| A.Q=92 kJ | B.Q< 92 kJ | C.Q> 92 kJ | D.Q=194kJ |