已知某链状有机物A的相对分子质量为72,根据下列条件回答下列问题(1)若该有机物只由碳、氢元素组成,则A的分子式为___________________,
其一氯代物只有一种的A的结构简式为______________________。
(2)若A为烃的含氧衍生物,且分子中有支链,又能发生银镜反应,则A结构简式为:_________,写出它发生银镜反应的化学方程式:__________________________。
(3)若A为烃的含氧衍生物,且不能发生银镜反应,则A的结构简式:__________________。
(4)若A分子中无甲基,又无羟基,但能发生银镜反应,则A的结构简式:________________。
写出它与新制的氢氧化铜悬浊液反应的化学方程式:_____________________________。
(5)若A能与Na反应放H2,且能使溴水褪色,结构中无甲基,
则A结构简式为:__________________。(注:双键碳不能直接连-OH,该结构不稳定)
已知在25 ℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17。
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1 L溶液)S(AgX)、S(AgY)、S(AgZ)的大小顺序为_________________ _____________________________________________。
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)________(填“增大”“减小”或“不变”)。
(3)在25 ℃时,若取0.188 g的AgY(相对分子质量188)固体放入100 mL水中(忽略溶液体积的变化),则溶液中Y-的物质的量浓度为________。
(4)由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,________(填“能”或“不能”),理由为_______________________________。
现有下列电解质溶液:
①Na2CO3②NaHCO3③ ④CH3COONH4⑤NH4HCO3
④CH3COONH4⑤NH4HCO3
(1)在这五种电解质溶液中,既能与盐酸又能与烧碱溶液反应的是(填写序号)________。
(2)已知酸性:H2CO3> >
> 。常温下,物质的量浓度相同的①②③溶液,pH由大到小顺序为(填序号)________>________>________。
。常温下,物质的量浓度相同的①②③溶液,pH由大到小顺序为(填序号)________>________>________。
(3)写出⑤与足量NaOH溶液混合加热反应的离子方程式: __________________________________________________________________。
(4)已知常温下CH3COONH4溶液呈中性,根据这一事实推测⑤溶液的pH________7(填“>”“=”或“<”),理由是________________________。
等电子体原理的应用
⑴与OH-互为等电子体的一种分子为(填化学式);
⑵S于O可形成SO42-,
①SO42-的空间构型为(用文字描述);
②写出一种鱼SO42-互为等电子体的分子的化学式。
⑶BF4-的立体构型为。
可逆反应:aA(g)+ bB(g) cC(g)+ dD(g);根据图回答:
cC(g)+ dD(g);根据图回答: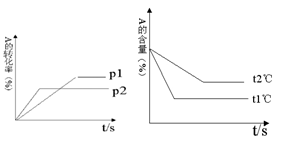
(1)压强 P1比P2(填大或小); (2)(a +b)比(c +d)(填大或小);
(3)温度t1℃比t2℃(填高或低);(4)正反应为反应。
7分)将标准状况下4.48 L的CO2通入适量的NaOH溶液中充分反应后,溶液中生成盐的质量为19.0 g。
(1)若要使生成的盐的质量变为25.2 g,则应继续向溶液中通入CO2多少克?(写出计算过程)
(2)向生成的19.0 g的盐溶液中加入一定量某物质,充分反应后,减压低温蒸发得到纯净的21.2 g Na2CO3固体。则:
①若只能加入0.05 mol某物质,则加入的物质可以是________或________。
②若只能加入0.10 mol某物质,则加入的物质可以是________或________。