高中化学实验中常见的使用温度计有如下3种情形①温度计的液泡浸没在液体反应物液面以下;②温度计的液泡置于水浴中;③温度计的液泡置于蒸馏烧瓶的支管口处。下列实验使用温度及正确的是……( )
| A.苯的硝化反应---① | B.酒精和浓硫酸混合加热制乙烯---① |
| C.测定硝酸钾在水中的溶解度---③ | D.分离苯和硝基苯的混合物---② |
常温下,下列溶液中,能大量共存的一组离子是
| A.pH=1的溶液中:NH4+、Fe2+、SO42-、Cl- |
| B.通入SO2气体的溶液中:Ca2+、I-、ClO-、NO3- |
| C.c(Fe3+)=" 0.1" mol•L-1的溶液中:Na+、I-、SCN-、SO42- |
| D.由水电离出的c(H+)=1.0×10-13 mol•L-1的溶液中:Na+、HCO3-、Cl-、Br- |
氨基钠和氢化钠与水反应的化学方程式如下:①NaNH2+H2O==NaOH+NH3↑②NaH+H2O==NaOH+H2↑,下列叙述正确的是
| A.氨基钠和氢化钠与盐酸反应都只生成一种盐 |
| B.方程式②中,每生成1mol H2转移1 mol电子 |
| C.氨基钠和氢化钠的晶体中都只含离子键 |
| D.方程式①中,氨基钠是还原剂 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大,X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,R与Y处于同一主族,Z是短周期中金属性最强的金属元素,W的最高价氧化物对应水化物能与Z、R的最高价氧化物对应水化物均反应生成盐和水。下列说法正确的是
| A.元素Y、Z、W的简单离子具有相同的电子层结构,其半径依次增大 |
| B.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| C.元素X与元素Y能形成两种化学键类型完全相同的化合物 |
D.元素X、Z形成化合物的电子式可以表示成 |
下列有关化工生产的叙述中,正确的是
| A.工业上可用氯化钠制备化肥NH4Cl |
| B.氯碱工业中,电解槽的阳极区产生NaOH |
| C.在接触室被氧化成SO3,SO3在吸收塔内被水吸收制成浓硫酸 |
| D.工业上用石英制太阳能电池,在高温下用铝热法炼铁制备钢材 |
85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖。颁奖理由是“因为发现青蒿素── 一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图)说法错误是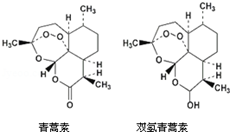
| A.青蒿素和双氢青蒿素互为同分异构体 |
| B.由青蒿素制备双氢青蒿素的反应属还原反应 |
| C.青蒿素的分子式为C15H22O5 |
| D.青蒿素分子中含有过氧链和酯基、醚键 |