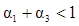下列说法中正确的是……( )
| A.分散系一定是混合物 |
| B.浊液一定可以用过滤的方法分离 |
| C.任何物质的溶解度总是随温度的升高而增大 |
| D.任何溶胶加入可溶性电解质后,都能使胶体微粒凝聚成较大颗粒形成沉淀而析出。 |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.用含0.1mol FeCl3的溶液与足量沸水反应制得的Fe(OH)3胶体中胶粒数为0.1NA |
| B.0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA |
| C.46g NO2和N2O4的混合气体中含N原子总数为NA |
| D.等物质的量的NH4+和OH-含电子数均为10NA |
下列说法正确的是
| A.向海水中加入明矾可以使海水淡化,用于解决淡水供应危机 |
| B.将地沟油回收再加工为食用油,以减缓水体富营养化 |
| C.大力推广农作物的生物防治技术,以减少农药的使用 |
| D.用聚氯乙烯代替木材,生产包装盒、快餐盒等,以减少木材的使用 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)  CO2(g)+H2(g) , 反应过程中测定的部分数据见下表(表中t1>t2): 下列说法正确的是
CO2(g)+H2(g) , 反应过程中测定的部分数据见下表(表中t1>t2): 下列说法正确的是
| 反应时间/min |
n(CO)/mol |
H2O/ mol |
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
0.20 |
A.反应在t1min内的平均速率为v(H2)=0.40/t1 mol·L-1·min-1
B.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小
D.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=0.40 mol
可逆反应①X(g)+2Y(g)
 2Z(g) 、②2M(g)
2Z(g) 、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示,下列判断正确的是
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示,下列判断正确的是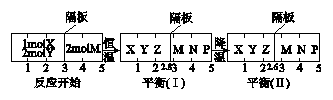
| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时,X的转化率为5/11 |
| C.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15 |
| D.在平衡(I)和平衡(II)中M的体积分数相等 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:下列说法正确的是
(已知N2(g)+3H2(g) 2NH3(g)
2NH3(g)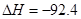 kJ·mol
kJ·mol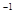 )
)
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1mol N2、3mol H2 |
2mol NH3 |
4mol NH3 |
NH3的平衡浓度(mol·L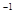 ) ) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出akJ |
吸收bkJ |
吸收ckJ |
| 体系压强(Pa) |
p1 |
p2 |
p3 |
| 反应物转化率 |
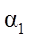 |
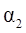 |
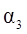 |
A.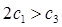 B.a+b>92.4C.
B.a+b>92.4C.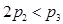 D.
D.