用pH试纸测定某无色溶液的pH时,规范的操作是……( )
| A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 |
| B.将溶液倒在pH试纸上,跟标准比色卡比较 |
| C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较 |
| D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较 |
在25℃和1.01×105Pa时,2N2O5(g)=4NO2(g) + O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A.是吸热反应 | B.是放热反应 | C.是熵减反应 | D.是熵增效应大于能量效应 |
下列有关“电离平衡”的叙述正确的是()
| A.电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等 |
| B.电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是静态平衡 |
| C.电离平衡是相对的、暂时的外界条件改变时,平衡就会发生移动 |
| D.电解质达到电离平衡后,各种离子的浓度相等 |
下列说法正确的是()
| A.物质的化学变化都伴随着能量变化 |
| B.凡是吸热反应都需要加热 |
| C.任何反应中的能量变化都表现为热量变化 |
| D.拆开旧化学键吸收的能量一定大于形成新化学键放出的能量 |
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是()
| 选项 |
A |
B |
C |
D |
| 实验项目 |
除去KCl中少量的MnO2 |
用10mol/L的盐酸配制100mL0.1mol/L的盐酸 |
用氯化钠溶液制备氯化钠晶体 |
除去CO2气体中的HCl |
| 实验仪器 或装置 |
烧杯、玻璃棒、漏斗 |
100mL容量瓶、玻璃棒、烧杯 |
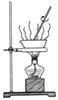 图1 |
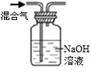 图2 |
用NA表示阿伏加德罗常数,下列叙述中正确的是()
| A.1 mol NH3中含有中子数为7NA个 |
| B.标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C.2 g氢气所含质子数是NA |
| D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |