下列说法正确的是( )
| A.二氧化硅溶于水显酸性 |
| B.二氧化碳通入水玻璃可得原硅酸 |
| C.因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸酸性比碳酸强 |
| D.二氧化硅是酸性氧化物,不溶于任何酸 |
在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。又知AgCl的Ksp=1.8×10-10。下列说法不正确的是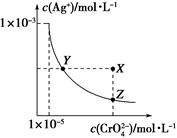
| A.t ℃时,Ag2CrO4的Ksp为1×10-11 |
| B.饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点 |
| C.t ℃时,Y点和Z点时Ag2CrO4的Ksp相等 |
| D.t ℃时,将0.01mol·L-1AgNO3溶液滴入20mL0.01mol·L-1KCl和0.01mol·L-1K2CrO4的混合溶液中,Cl-先沉淀 |
下列有关溶液中微粒的物质的量浓度关系正确的是
A.某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A)
B.0.1mol·L-1CH3COONa溶液与0.05mol·L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+)
C.物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:c(CN-)+2c(OH-)=2c(H+)+c(HCN)
D.0.1mol·L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3·H2O)+c(Fe2+)=0.3mol·L-1
室温时,向20mL0.1mol·L-1的醋酸溶液中不断滴入0.1mol·L-1的NaOH溶液,溶液的pH变化曲线,如图2所示。在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是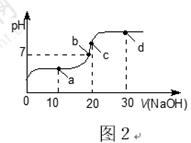
| A.a点时:c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.b点时:c(Na+) ="c(" CH3COO-)>c(H+)="c(" OH-) |
| C.c点时:c(OH-)=c(CH3COOH) +c(H+) |
| D.d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.在pH=1的溶液中:K+、Na+、SO42–、HCO3- |
| B.在0.1mol·L-1Na2CO3溶液中:Al3+、K+、NO3-、SO42- |
| C.在0.1mol·L-1FeCl3溶液中:K+、NH4+、I-、SCN- |
| D.在c(H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- |
一定温度下,满足下列条件的溶液一定呈酸性的是
| A.c(H+)>c(OH-)的任意水溶液 | B.加酚酞后显无色的溶液 |
| C.pH=6的某溶液 | D.能与金属Al反应放出H2的溶液 |