分别处于第2、3周期的主族元素A和B,它们离子的电子层相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别为
A.m、n
B.3、7
C.m-2、10-n
D.m+2、10+n
下列化学用语中表达正确的是
A.四氯化碳的电子式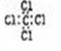 |
B.C2 H4的结构简式:CH2CH2 |
C.环已烷的结构简 |
D.次氯酸的结构式:H-Cl-O |
芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1mol H2,若1 mol C与NaHCO3完全反应,也产生1 mol气体,E可以使溴的四氯化碳溶液褪色。
(1)③的反应类型是,D的结构简式是。
(2)E中所含官能团的名称为。
(3)写出对应的化学方程式
反应①;
反应④;
反应⑤。
(4)现有C和E的混合物n mol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2 a L(标准状况)、H2O b g,则C、E混合物中含E的物质的量的计算式为:。
某高聚物的单体A(C11H12O2)可发生以下变化:
已知: C的烃基部分被取代生成的一氯代物D有两种;F的分子式为C7H8O,含有苯环,但与FeCl3溶液不显色。请回答:
(1)F分子中含有的官能团结构简式是。
(2)由A生成B和F的反应类型为(选填序号)____。
①氧化反应 ②取代反应 ③水解反应 ④消去反应
(3)B的结构简式是____。
(4)分子式为C7H8O,含有苯环的同分异构体除F外还有__ __种。
(5)写出下列方程式
① 由A生成B和F ______; ② B → C ______ ;
③A在一定条件下生成高聚物 ________。
有机物甲的分子式为C9H18O2,在酸性条件下甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有()
| A.14种 | B.8种 | C.18种 | D.16种 |
如图所示装置进行实验,将液体A逐滴加入到固体B中, 下列叙述中错误的是 
| A.实验中仪器C可起到防止倒吸的作用 |
| B.若A为醋酸,B为贝壳(粉状),D中盛C6H5ONa溶液,则D中溶液变浑浊 |
| C.若A为浓氨水,B为生石灰,D中盛AgNO3溶液,则D中无现象 |
| D.若A为食盐水,B为电石,D中盛KMnO4酸性溶液,则D中溶液紫红色褪色 |