某气体的摩尔质量为M g·mol-1,Na表示阿伏加德罗常数的值,在一定温度和压强下体积为V L的气体所含有的分子总数为X,则 表示( )
表示( )
| A.以g为单位V L该气体的质量 | B.每升气体中所含的分子数 |
| C.以g为单位1 L该气体的质量 | D.以L为单位1 mol该气体的体积 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,是我国经常使用的电动车的电池。电池反应为:FePO4 + Li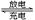 LiFePO4,该电池的正极材料是FePO4,负极材料是石墨,含Li+的导电固体为电解质,下列有关该电池的说法正确的是
LiFePO4,该电池的正极材料是FePO4,负极材料是石墨,含Li+的导电固体为电解质,下列有关该电池的说法正确的是
| A.可以加入硫酸以提高电解质的导电率 |
| B.放电时电池内部Li+向负极移动 |
| C.充电过程中,电池正极材料的质量减少 |
| D.放电时电池正极反应为:FePO4 + Li++ e— = LiFePO4 |
我国拥有完全自主产权的氢氧燃料电池车已经在北京奥运会期间为运动员服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
| A.工作一段时间后,负极周围的pH增大 |
| B.工作后,电解液中的KOH的物质的量不变 |
| C.该燃料电池的总反应式为:2H2 + O2 = 2H2O |
| D.用该电池电解CuCl2溶液,产生7.1g Cl2时,电子转移0.1mol |
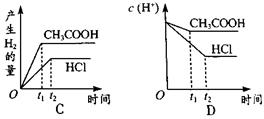
向体积都为1L,pH都等于2的盐酸和醋酸溶液中投入0.65gZn,则下图中比较符合客观事实的曲线是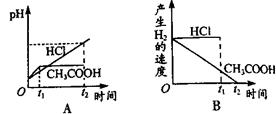
恒温条件下,在CH3COONa的稀溶液中分别加入下列的物质,能使c(CH3COO—)/c(Na+)比值一定增大的是
| A.固体NaOH | B.固体KOH | C.固体NaCl | D.冰醋酸 |
在常温下Cu(OH)2的Ksp=2×10-20。某CuSO4溶液中c(Cu2+)=0.02mol/L,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液中加入碱溶液来调整溶液的pH,应该使溶液的pH大于
| A.8 | B.9 | C.4 | D.5 |