在500 mL CuSO4和Fe2(SO4)3的混合溶液中加入21.7 g铁粉,待反应完全后,得到16.8 g残留固体。在滤液中加入400 mL 4 mol·L-1的BaCl2溶液,恰好使溶液中的 完全沉淀。求原混合物中CuSO4和Fe2(SO4)3的物质的量浓度。
完全沉淀。求原混合物中CuSO4和Fe2(SO4)3的物质的量浓度。
过氧化钠与水反应可以制取氧气,现欲制取标准状况下1.12L的氧气,则至少需要过氧化钠的质量为,产生NaOH的物质的量为。
(1)标准状况下,67.2LCO2的物质的量是mol,
质量为g,含有个氧原子。
(2)0.6mol O2与0.4mol O3质量之比为,分子个数之比为。
某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示: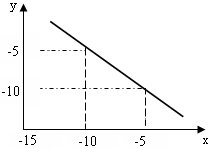
(1)该温度下水的离子积为。
(2)该温度下0.01 mol/L的NaOH溶液pH为。
(10分)把一定质量的镁、铝混合物投入到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。则:
(1)金属铝的质量为_______。(2)a的取值范围是________。
(3)盐酸的体积是ml。(4)n(Mg)/n(Al)的最大值是________。
(5)80~90ml对应反应的离子方程式。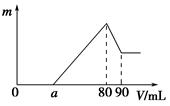
(本题共14分)已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2 2CuO
2CuO 4NO2↑
4NO2↑ O2↑开始分解,至250℃分解完全。(其中2NO2
O2↑开始分解,至250℃分解完全。(其中2NO2 N2O4,2NO2
N2O4,2NO2 2NO
2NO O2等反应忽略不计)。
O2等反应忽略不计)。
800℃时,4CuO 2Cu2O
2Cu2O O2↑ 开始分解,至1000℃以上分解完全。
O2↑ 开始分解,至1000℃以上分解完全。
54.取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是(填分子式),体积(标准状况)为;将吸收液加水稀释到100mL,此溶液中 的物质的量浓度为。
的物质的量浓度为。
55.取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O 4Cu
4Cu O2↑
O2↑
56.取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
57.取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中n (Cu2O) n (Cu)
n (Cu) x。将此混合物溶于足量的稀硫酸中(Cu2O
x。将此混合物溶于足量的稀硫酸中(Cu2O 2H
2H
 Cu
Cu Cu
Cu
 H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。