少量的碘化物可用以下方法进行测定,其步骤如下:
①在中性或弱酸性介质中先用过量的Br2,将试样中的I-氧化成 ;
;
②煮沸①所得溶液以除去过量的Br2,然后在酸性条件下加入过量的KI溶液,将 还原为I2;
还原为I2;
③在②中加淀粉作指示剂,用Na2S2O3标准溶液滴定(2Na2S2O3+I2====2NaI+Na2S4O6)。
通过上述步骤可测得碘化物中I-的含量:
(1)写出步骤①②中发生反应的离子方程式:
①__________________________________________,
②__________________________________________。
(2)若样品中有1 mol I-,则最后耗用Na2S2O3的物质的量是多少?
(3)若在测定时,准确量取含KI的样品溶液25.00 mL,终点时耗用0.050 mol·L-1 Na2S2O3溶液20.06 mL,试计算样品溶液中KI的含量(g·L-1)。
某温度下的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x与y的关系如图所示: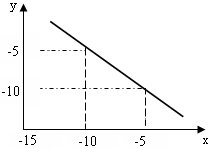
(1)该温度下水的离子积为。
(2)该温度下0.01 mol/L的NaOH溶液pH为。
(10分)把一定质量的镁、铝混合物投入到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。则:
(1)金属铝的质量为_______。(2)a的取值范围是________。
(3)盐酸的体积是ml。(4)n(Mg)/n(Al)的最大值是________。
(5)80~90ml对应反应的离子方程式。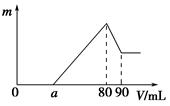
(本题共14分)已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2 2CuO
2CuO 4NO2↑
4NO2↑ O2↑开始分解,至250℃分解完全。(其中2NO2
O2↑开始分解,至250℃分解完全。(其中2NO2 N2O4,2NO2
N2O4,2NO2 2NO
2NO O2等反应忽略不计)。
O2等反应忽略不计)。
800℃时,4CuO 2Cu2O
2Cu2O O2↑ 开始分解,至1000℃以上分解完全。
O2↑ 开始分解,至1000℃以上分解完全。
54.取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是(填分子式),体积(标准状况)为;将吸收液加水稀释到100mL,此溶液中 的物质的量浓度为。
的物质的量浓度为。
55.取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O 4Cu
4Cu O2↑
O2↑
56.取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
57.取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中n (Cu2O) n (Cu)
n (Cu) x。将此混合物溶于足量的稀硫酸中(Cu2O
x。将此混合物溶于足量的稀硫酸中(Cu2O 2H
2H
 Cu
Cu Cu
Cu
 H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
某温度下,在装有催化剂的容积为2 L的反应容器中,充入SO2和O2各4 mol ,充分反应5 min后达到平衡,测得反应容器内混合气体的压强为原来的80 %。回答下列问题:
(1)用O2的浓度变化表示该反应的化学反应速率。
(2)求SO2的转化率。
(3)求该反应的平衡常数。
(7分)取含MnO2的软锰矿石27.86g跟足量浓盐酸反应(杂质不参与反应),制得17.75gCl2,求(1)这种软锰矿石中MnO2的百分含量。(2)求被氧化的HCl的质量。