在60gSiO2晶体中,含有Si-O键的物质的量为 ( )
| A.1mol | B.2mol | C.3mol | D.4mol |
可以证明可逆反应 已达到平衡状态的是
已达到平衡状态的是
①一个N N键断裂的同时,有6个N-H键断裂
N键断裂的同时,有6个N-H键断裂
②
③保持其他条件不变时,体系压强不再改变;
④NH3、N2、H2的体积分数都不再改变;
⑤恒温恒容时,混合气体质量保持不变;
| A.②③④ | B.①②④ |
| C.①③④ | D.③④⑤ |
已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol/L CH3COOH溶液中逐滴加入0. 1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是
A.a点表示溶液中c(CH3COO-)约为10 mol/L mol/L |
| B.b点表示的溶液中c(Na+)>c(CH3COO-) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.d点表示的溶液中 大于K 大于K |
汽车尾气净化中的一个反应如下:
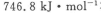 在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是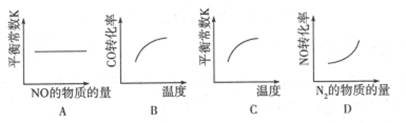
已知反应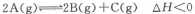 ,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为
,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为
A.减小容器容积B.增大容器容积
C.减小B的浓度D.降温
下列叙述正确的是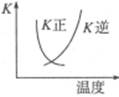
| A.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
B. 的正、逆反应的平衡常数K随温度的变化可用上图表示 的正、逆反应的平衡常数K随温度的变化可用上图表示 |
C.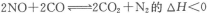 ,常温下该反应一定能自发进行 ,常温下该反应一定能自发进行 |
| D.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小 |