下列离子方程式中属于水解反应,而且可使溶液酸性的是
A.HS-+H2O S2-+H3O+ S2-+H3O+ |
B.SO3+2H2O HSO4-+H3O+ HSO4-+H3O+ |
C.HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
D.NH4++2H2O NH3·H2O+H3O+ NH3·H2O+H3O+ |
O3也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀毒消毒能力。常温常压下发生反应如下:反应①O3⇌O2+[O]△H>0 平衡常数为K1;
反应②[O]+O3=2O2△H<0 平衡常数为K2;
总反应:2O3=3O2△H<0 平衡常数为K
下列叙述正确的是()
| A.升高温度,K增大 |
| B.K=K1+K2 |
| C.压强增大,K2减小 |
| D.适当升温,可提高消毒效率 |
下列溶液中有关微粒的物质的量浓度关系正确的是()
A.NaHRO3溶液中(R表示S或C):c(Na+) >c(HRO3-)>c(OH-)>c(H+)>c(RO32-)
B.常温下将醋酸钠、盐酸两溶液混合后呈中性,则混合溶液中:c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<③<②
D.等体积等物质的量浓度的NaClO溶液与NaCl溶液中离子总数:N前﹥N后
常温下,一定量冰醋酸加水稀释过程中,溶液的导电性如下图所示。下列说法正确的是()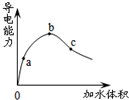
| A.pH值:b>a>c |
| B.与锌反应起始速率:a=b=c |
| C.水电离的c(H+) c>a>b |
| D.加入足量的NaHCO3固体,产生气体体积:a>b>c |
在含有nmolFeI2的溶液中通入Cl2,有xmolCl2发生反应,下列说法正确的是()
| A.当x≤0.5n时,反应的离子方程式为:2Fe2++Cl2===2Fe3++2Cl- |
| B.当x≥n时,反应的离子方程式为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| C.当Fe2+和I-都被氧化时,x的最小值须大于0.5n |
| D.当x=n时,反应后氧化产物的物质的量为nmol |
溶液中含有较高浓度的NH4+、F-、HSO3-、K+等离子,向其中加入少量NaClO固体后,溶液中离子数目肯定增加的是()
| A.F- | B.ClO- | C.HSO3- | D.NH4+ |