含CrO72-的工业酸性废水会造成铬污染,排放前要先进行如下处理:①先将Cr2O72-还原成Cr3+②往废水中加入适量NaCl后,以Fe为电极进行电解,同时鼓入空气。从而使溶液的pH不断升高,废水由酸性转化为碱性,Cr3+即变为不溶性氢氧化物除去。处理该废水的过程中,溶液pH不断升高的原因是下列反应事实中的
| A.电解时废水体积不断减小 |
| B.电解时H+在阴极处被还原 |
| C.作为阳极的Fe不断溶解 |
| D.Cr2O72-转化为Cr3+没有消耗H+ |
A、B、C、D都是含碳、氢、氧的单官能团化合物,A水解得到B和C,B氧化可以得到C或D,D氧化也可得到C。若M(x)表示x的摩尔质量,则下式中正确的是:
A.M(A)=M(B)+M(C) B.2M(D)=M(B)+M(C)
C.M(B)<M(D)<M(C) D.M(D)<M(B)<M(C)
下列分子式表示的物质一定是纯净物的是
| A.C5H10 | B.C7H8 | C.CH4O | D.C2H4Cl2 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。下列说法不正确的是
| A.淀粉水解的最终产物能发生银镜反应 |
B.淀粉和纤维素均可用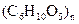 表示,因此它们互为同分异构体 表示,因此它们互为同分异构体 |
| C.蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水 |
| D.脂肪能发生皂化反应,生成甘油和高级脂肪酸钠 |
目前冰箱中使用的致冷剂是氟里昂(二氯二氟甲烷),其同分异构体有
| A.不存在同分异构体 | B.2种 | C.3种 | D.4种 |
下列各物质中,不能发生水解反应的是
| A.果糖 | B.油脂 | C.纤维素 | D.酶 |