已知浓盐酸和次氯酸钙能发生如下反应:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是( )
①CO2 ②HCl ③H2O ④O2
| A.①②③ | B.②③④ | C.②③ | D.①④ |
下列各组混合物中,不论两种物质以何种比例混合,只要总质量一定,经过完全燃烧后,产生的CO2质量不变的是()
| A.乙炔和甲苯 | B.丙烯和丙烷 | C.乙醇和丙酸 | D.甲醛与葡萄糖 |
由溴乙烷制取乙二醇,依次发生反应的类型是()
| A.取代、加成、水解 | B.消去、加成、取代 |
| C.水解、消去、加成 | D.消去、水解、取代 |
某烯烃与H2加成后的产物是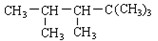 ,则该烯烃的结构式可能有()
,则该烯烃的结构式可能有()
| A.4种 | B.3种 | C.2种 | D.1种 |
某有机物的结构简式如图所示,其名称正确的是()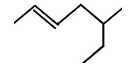
| A.5-乙基-2-己烯 | B.3-甲基庚烯 |
| C.3-甲基-5-庚烯 | D.5-甲基-2-庚烯 |
一次区分乙酸、乙醇、苯、四氯化碳四种液体的试剂是()
| A.H2O | B.溴水 | C.新制Cu(OH)2 | D.酸性高锰酸钾溶液 |