下列各物质中,按熔沸点由低到高排列正确的是
A.O2、S、Hg B.SO2、H2SO4、SiO2
C.N2、P、As D.SiC、NaCl、SO3
下列分类或归类正确的是:
①铝热剂、纯净矿泉水、冰水混合物均为混合物
②NaOH、HD、IBr均为化合物
③明矾、烧碱、硫酸均为强电解质
④C60、金刚石、石墨均为碳的同素异形体
⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体
A.①②③⑤ B.③④⑤ C.②④⑤ D.③④
已知a g气体X2中含有b个X原子,那么c g该气体在0℃、1.01×105 Pa条件下的体积是(NA表示阿伏加德罗常数的值)
A.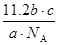 L L |
B. L L |
C.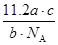 L L |
D. L L |
下列各组离子以适当比例混合,可以形成无色透明碱性溶液的是
| A.Na+、 Ba2+、OH-、SO42- | B.Ag+、NH4+、OH-、NO3- |
| C.Mg2+、Na+、AlO2-、OH- | D.MnO4-、Al3+、SO42-、Cl- |
下列离子方程式正确的是
A.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2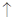 |
| B.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
C.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-=BaSO4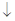 +H2O +H2O |
D.用小苏打类药物治疗胃酸过多:HCO3-+H+=CO2 +H2O +H2O |
下列物质中,分子物质的量最多的是(相对原子质量 H—1 O—16)
| A.1molN2 | B.1g H2 | C.0.1NAO2 | D.4℃时,20mL水 |