制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现
①Si(s)+3HCl(g)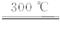 SiHCl3(s)+H2(g) ②SiHCl3+H2
SiHCl3(s)+H2(g) ②SiHCl3+H2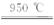 Si+3HCl
Si+3HCl
对上述两个反应的下列叙述中,错误的是( )
| A.两个反应都是置换反应 |
| B.反应②不是置换反应 |
| C.两个反应互为可逆反应 |
| D.两个反应都是氧化还原反应 |
下列分子中, 所有原子不可能处在同一平面上的是
| A.乙烷 | B.乙烯 | C.氯乙烯(CH2=CHCl) | D.苯 |
某烷烃含有200个氢原子,那么该烃的分子式是
| A.C97H200 | B.C98H200 | C.C99H200 | D.C100H200 |
两种气态烃组成的混合气体0.1mol,完全燃烧得0.15 mol CO2和3.6 g H2O,下列关于该混合气体的说法正确的是
| A.一定有乙烯 | B.一定没有乙烯 | C.一定有甲烷 | D.一定没有乙烷 |
乙醇分子中不同的化学键,如右图:关于乙醇在各种反应中、断裂键的说法不正确的是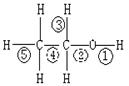
| A.乙醇和钠反应,键①断裂 |
| B.在铜催化下和O2反应,键①③断裂 |
| C.乙醇制乙烯时,键②⑤断裂 |
| D.在铜催化下和O2反应,键①②断裂 |
把质量为mg的铜丝灼烧变成黑色,立即放入下列物质中,使铜丝变成红色,而且质量仍为mg的是
| A.稀H2SO4 | B.C2H5OH | C.CH3COOH溶液 | D.CO |