由于候鸟的迁徙。“禽流感”在部分国家和地区出现新一轮的爆发。从烹调香料八角中提取到的莽草酸是制取抗禽流感药物达菲的基本原料,其结构如右,下列对莽草酸的说法正确的是( )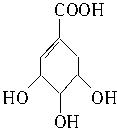
| A.分子式为C7H10O5 | B.莽草酸是芳香族化合物 |
| C.莽草酸遇FeCl3溶液变紫色 | D.1mol莽草酸与足量钠反应可产生4mol氢气 |
茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是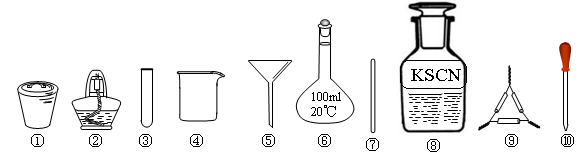
| A.将茶叶灼烧灰化,选用①、②和⑨ |
| B.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ |
| C.过滤得到滤液,选用④、⑤和⑦ |
| D.检验中滤液中的Fe3+,选用③、⑧和⑩ |
下列实验操作与预期的实验目的或结论均正确的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
向FeCl3溶液中通入Cl2,然后滴加KSCN溶液 |
验证Cl2的氧化性比Fe3+强 |
| B |
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中不一定含有SO42- |
| C |
用洁净的Pt丝蘸取某溶液进行焰色反应,火焰呈黄色 |
该溶液中一定含有Na+,一定无K+ |
| D |
直接加热MgCl2·6H2O晶体 |
获取无水MgCl2固体 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5 MnO2+2 Ag+2 NaCl=Na2Mn5O10+2 AgCl。下列关于“水”电池的说法不正确的是
| A.AgCl是还原产物 |
| B.负极的电极反应为:Ag+Cl- — e-=AgCl |
| C.Na+不断向“水”电池的正极移动 |
| D.每生成1mol Na2Mn5O10转移2mol电子 |
在含有FeCl3、FeCl2、AlCl3、NaCl的溶液中,加入足量的NaOH溶液,在空气中充分搅拌反应后再加入过量的稀盐酸,溶液中离子数目减少的是
| A.Na+ | B.Fe3+ | C.Al3+ | D.Fe2+ |
Fe2O3、ZnO、CuO的固体混合粉末a g,在加热条件下用足量CO还原,得到金属混合物4.82g,
将生成的CO2气体用足量的澄清石灰水吸收后,产生l0.00g白色沉淀,则a 的数值为
| A.4.92 | B.6.42 | C.7.18 | D.14.82 |