| A.107 | B.5.56×108 |
| C.1.0×10-14 | D.55.6 |
下列电子式书写正确的是
| A.∶N∶∶∶N∶ | B. |
C.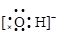 |
D.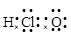 |
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化
H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.H2O2 | B.IO3 | C.MnO4 | D.HNO2 |
下列条件下,两种气体所含的原子数一定相等的是
| A.同质量、不同密度的N2和CO | B.同温度、同体积的H2和N2 |
| C.同体积、同密度的C2H6和NO | D.同压强、同体积的N2O和CO2 |
下列叙述正确的是
①一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路
②一定温度和压强下,气体体积主要由其分子的物质的量决定
③气体摩尔体积是指单位物质的量气体所占的体积,其单位是L
④在同温同体积时,气体的物质的量越大,则压强越大
⑤蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
⑥标准状况下,将lg铝片投入20mL 18mol/L的硫酸中,铝片完全溶解
| A.①②④ | B.①③⑤ | C.②③⑥ | D.②④⑤ |
设NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.1 mol Na2O2中含有的阴离子数为0.2NA |
| B.标准状况下,由H2O2制得2.24LO2转移的电子数目为0.4NA |
| C.常温常压下,8gO3含有4 NA个电子 |
| D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA |