下列关于热化学反应的描述中正确的是
| A.已知H+(aq)+OH-(aq)=H2O(1);ΔH=-57.3kJ·mol-1, 则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3)kJ·mol-1 |
| B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+1/2O2(g)=CO2(g)+ 2H2(g);ΔH=-192.9 kJ·mol-1,则CH3OH的燃烧热为192.9 kl·mol-1 |
| C.H2(g)的燃烧热是285.8 kJ·mol -1,则2H2O(g)=2H2(g)+O2(g); ΔH =" +571.6" kJ·mol -1 |
| D.葡萄糖的燃烧热是2 800 kJ·mol -1,则l/2C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(1); |
ΔH =" -1" 400 kJ·mol-1
下列各组物质的燃烧热相等的是
| A.碳和一氧化碳 | B.淀粉和纤维素 |
| C.1 mol碳和3 mol碳 | D.3 mol C2H2和1 mol C6H6 |
对处于化学平衡的体系,由化学平衡与化学反应速率的关系可知
| A.化学反应速率变化时,化学平衡一定发生移动 |
| B.化学平衡发生移动时,化学反应速率一定变化 |
| C.正反应进行的程度大,正反应速率一定大 |
| D.只有在催化剂存在条件下,才会发生化学反应速率变化而化学平衡不移动的情况 |
某实验小组学生按照课本实验要求,用50 mL 0.5 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量计算中和热。下列说法正确的是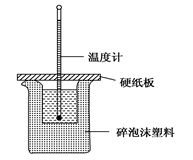
| A.实验过程中没有热量损失 |
| B.图中实验装置缺少环形玻璃搅拌棒 |
| C.烧杯间填满碎泡沫塑料的作用是固定小烧杯 |
| D.酸或碱的物质的量越大,所测中和热的数值越大 |
工业制硫酸的第一步反应,可用化学方程式表示如下:4FeS2+11O2=2Fe2O3+8SO2
对此反应下列说法中正确的是()
| A.FeS2既是氧化剂又是还原剂 |
| B.O2只做氧化剂 |
| C.氧化产物只有Fe2O3 |
| D.4molFeS2发生反应时,反应中共有22mol电子转移 |
某无色溶液中加入氯化钡后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中
| A.一定含有SO42- | B.一定含有Ag+ |
| C.可能含有SO42-或Ag+ | D.一定含有Ag+、SO42- |