生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是
①人的皮肤在强紫外线的照射下将会失去生理活性
②用甲醛溶液浸泡海产品保鲜
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④棉花和木材的主要成分都是纤维素,禽类羽毛和蜘蛛丝的主要成分都是蛋白质
⑤蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
| A.①④⑤ | B.②③④ | C.①②④⑤ | D.全部 |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是
| A.植物油不能使溴的四氯化碳溶液褪色 |
| B.淀粉水解的最终产物是葡萄糖 |
| C.葡萄糖能发生氧化反应和水解反应 |
| D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
奥运吉祥物福娃,其外材为纯羊毛线,内充物为无毒的聚酯纤维(如下图所示),下列说法正确的是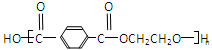
| A.羊毛与聚酯纤维的化学成分相同 |
| B.聚酯纤维和羊毛一定条件下均能水解 |
| C.该聚酯纤维的单体为对苯二甲酸和乙醇 |
| D.聚酯纤维属于纯净物 |
某有机物A是农药生产中的一种中间体,其结构简式如下图。则下列叙述正确的是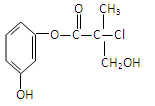
| A.有机物A属于芳香烃 |
| B.有机物A可以和Br2的CCl4溶液发生加成反应 |
| C.有机物A和浓硫酸混合加热,可以发生消去反应 |
| D.1molA和足量的NaOH溶液反应,最多可以消耗4mol NaOH |
花青苷是引起花果呈现颜色的一种花色素,广泛存在于植物中。它的主要结构在不同pH条件下有以下存在形式:
下列有关花青苷说法不正确的是( )
| A.花青苷可作为一种酸碱指示剂 |
| B.I和II中均含有二个苯环 |
| C.I和II中除了葡萄糖基外,所有碳原子可能共平面 |
| D.I和II均能与FeCl3溶液发生显色反应 |