下图为从反面看到的某套实验装置示意图,无法看到实验说明,加热装置已经省略。
甲同认为此套装置用于合成物质X,E处冰水冷却的U型管中有固体X出现;乙同认为此套装置用于合成物质Y,E处冰水冷却的U型管中有红棕色气体Y生成,并且越接近U型管底部颜色越浅。对于A处,甲认为有加热装置,乙认为没有。
(1)事实上此装置所附实验说明符合甲同的推断,那么X的化式是 ,C装置中盛放的液体药品是 。
(2)甲同方案中为了提高A装置产物的转化率,可以增大B装置产物的通入量。要知道A、B两个装置产物的通入量哪个大,可通过观察 得知。
(3)若要用上述装置完成乙同所认为的实验,C处所起作用与合成X时所起作用一致,那么C处的广口瓶应改为 ,所装药品为 。
(4)写出乙同认为的D装置中发生反应的化方程式 。为什么此时U型管中的红棕色气体越接近管底颜色越浅?
以下是实验室制取氯气的装置,在图中饱和食盐水的作用是_____________,
浓硫酸的作用是____________________,F中盛放的溶液是__________________________,
起的作用是_____________________________。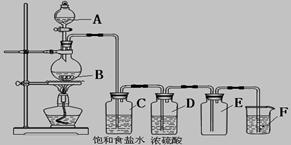
为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中。
| 实验要求 |
化学试剂 |
| 1.检验酒精中是否有水 |
|
| 2.区别CH4和C2H4两种无色气体 |
|
| 3.验证味精是否有食盐 |
|
| 4.除去Fe2O3中的Al2O3 |
供选择的化学试剂:
A.酸性高锰酸钾B.硝酸银溶液和硝酸C.氢氧化钠溶液D.无水硫酸铜粉末
欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL。试回答下列问题:
(1)你所需要量取的浓硫酸的体积为mL。
(2)除下图中仪器①②外,本实验还需要用到的玻璃仪器有:胶头滴管、、。
下图是某同学转移溶液的示意图,请改正图中的错误:。
(3)配制过程中,造成浓度偏高的操作可能有(填序号)。
| A.容量瓶用蒸馏水洗后未干燥 |
| B.量筒用蒸馏水洗后未干燥 |
| C.未用水洗涤溶解过浓硫酸的烧杯 |
| D.用量筒量取浓硫酸时,俯视读数 |
E.定容时,俯视液面加水至刻度线
F.向容量瓶中转移浓溶液时不慎有液滴掉在容量瓶外面
G.将烧杯中溶解后的溶液立即转移入容量瓶,然后再加蒸馏水至刻度线
H.用胶头滴管向容量瓶中加水时,不慎超过刻度线,又用胶头滴管从容量瓶中吸出部分溶液,使液面的最低点刚好与刻度线相切
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):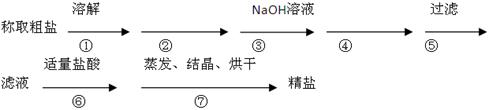
(1)步骤②中应加入的试剂是溶液,判断此试剂已加过量的方法是。
(2)步骤④中应加入的试剂是溶液,第④步中相关的离子方程式是。
(3)若将第⑤步和第⑥步颠倒,会对实验结果产生影响,其原因是。
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100g水 |
| 正丁醇 |
74 |
0.80 |
118.0 |
9 |
| 冰醋酸 |
60 |
1.045 |
118.1 |
互溶 |
| 乙酸正丁酯 |
116 |
0.882 |
126.1 |
0.7 |
请回答有关问题。
Ⅰ.乙酸正丁酯粗产品的制备
在A中加入11.5mL正丁醇和7.2mL冰醋酸,再加3~4滴浓硫酸,混合均匀,投入沸石。如图所示安装分水器、温度计及回流冷凝管,并在分水器中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。
(1)仪器A中发生反应的化学方程式为____________________________。有同学拟通过某种方法鉴定所得产物中是否含有杂质,可采用确定。
a.红外光谱法 b.1H核磁共振谱法 c.质谱法
(2)“反应中利用分水器将水分去”该操作的目的是:。
(3)反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是。
(4)可根据现象来判断反应完毕。
Ⅱ.乙酸正丁酯粗产品的精制
(5)将仪器A中的液体转入分液漏斗中,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是。
(6)再用10ml 10%Na2CO3溶液洗涤有机层,该步操作的目的是。
(7)将干燥后的产品蒸馏收集乙酸正丁酯产品时,应将温度控制在左右。