A、B两种化合物的溶解度曲线如图所示,现要用结晶法从A、B混合物中提取A(不考虑A、B共存时对各自溶解度的影响)。
取50g混合物,溶于100g热水,然后冷却至20℃。若要使A析出而B不析出。则混合物中B的质量分数(B%)最高不能超过多少?(写出推理及计算过程)
取Wg混合物。溶于100 g的热水,然后冷却至10℃若仍要使A析出而B不析出。请写出下列两种情况下,混合物中A的质量分数(A%)应满足什么关系式。(以W、a、b表示)
当W<a+b时,A%_____________
当W>a+b时, A%______________
为了测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
| A.冷却至室温后,在250mL容量瓶中定容配成250mL稀硫酸。 |
| B.用某仪器量取25.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
| C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为M mol/L的标准NaOH溶液装入碱式滴定管,调节液面记下开始读数为V1mL。 |
E、小心滴入NaOH标准溶液,边滴边摇动锥形瓶,滴定至恰好反应为止,记下读数为V2mL。
F、把锥形瓶移到碱式滴定管下,在锥形瓶下垫一张白纸。
G、用某仪器准确量取浓硫酸样品10.00 mL,在烧杯中用蒸馏水溶解。
就此实验操作完成下列填空:
⑴正确操作步骤的顺序(用编号字母填写)→ A → → →→ →。
⑵用来量取10.00mL浓硫酸的仪器是。用NaOH溶液润洗碱式滴定管的目的是。
⑶滴定中可选用的指示剂是。滴定中,目光应注视_____ ;判断滴定恰好完成的依据是____;读数时,目光与凹液面的最低处保持水平。
⑷某学生实验时用稀硫酸润洗了锥形瓶测定的浓度会偏_。(填“偏高”、“偏低”、“无影响”)
⑸该浓硫酸样品的浓度计算式为 ___________ 。
实验室迅速制备少量氯气可利用如下所示的反应
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O ; 当参加反应的氧化剂的物质的量是1mol时,回答下列问题:
(1)被氧化的还原剂的物质的量是多少?
(2)产生标准状况下的氯气的体积多少升?
实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①取25mL甲溶液,向其中缓慢滴入乙溶液15mL,共收集到112mL(标准状况)气体。
②取15mL乙溶液,向其中缓慢滴入甲溶液25mL,共收集到56mL(标准状况)气体。
(1)判断:甲是溶液,乙是溶液;(均填化学式)
(2)甲溶液的物质的量浓度为mol/L,乙溶液的物质的量浓度
为mol/L,(要求写出计算过程)。
(1)普通玻璃的成分Na2CaSi6O14,以氧化物形式可表示为;
(2)若要制备7.17吨该产品,其中需要石灰石、石英(利用率按75%计算)
各多少吨,并同时共产生标况下的温室效应气体CO2多少立方米?
工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:
2C4H10+5O2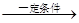 4CH3COOH+2H2O
4CH3COOH+2H2O
现用58吨丁烷为原料制取醋酸,求:
(1)理论上需要标准状况下的空气m3(设空气中O2、N2的体积分数分别为0.2、0.8),同时生成水吨。
(2)若生成的醋酸溶解在 生成的水中,所得醋酸的质量分数为%。
生成的水中,所得醋酸的质量分数为%。
(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且 ,需补充水y吨,则y与x的关系式为(用含x的代数式表示y);若不补充水,则m1+m2=。
,需补充水y吨,则y与x的关系式为(用含x的代数式表示y);若不补充水,则m1+m2=。