化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类比是相对的,如根据2Na2O2+2CO2= Na2CO3+ O2, 类2Na2O2+2SO2= Na2SO3+ O2是错误的,应该是Na2O2+SO2= Na2SO4。
|
下列各组类比中正确的是 ( )
A.由NH4Cl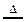 NH3↑+HCl↑,推测:NH4I NH3↑+HCl↑,推测:NH4I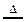 NH3↑+HI↑ NH3↑+HI↑ |
| B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO |
| C.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO,推测:CO2+NaClO+H2O=NaHCO3+HClO |
| D.由Na2SO3+2HCl=2NaCl+H2O+ SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+ SO2↑ |
在20℃时,某气态烃与氧气混合,装入密闭容器中,点燃爆炸后,又恢复到20℃,此时容器内气体的压强为反应前的一半,经NaOH溶液吸收后,容器内几乎成真 空,此烃的分子式可能是
空,此烃的分子式可能是
| A.CH4 | B.C2H6 | C.C7H16 | D.C3H8 |
25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
| A.c(NH4+)>c(SO42-) | B.c(NH4+)=c(SO42-) |
| C.c(NH4+)<c(SO42-) | D.c(OH-)+c(SO42-)=c(H+)+c (NH4+) |
下列说法正确的是
| A.两种物质的组成元素相同,各元素的质量分数也相同,则两者一定为同分异构体 |
B.分子式为CnH2n的 化合物,可能使酸性KMnO4溶液褪色,也可能不褪色 化合物,可能使酸性KMnO4溶液褪色,也可能不褪色 |
| C.通式相同,组成上相差一个或n个“CH2”原子团的化合物,一定互为同系物 |
| D.凡含有苯环的物质都是芳香烃 |
下列物质既能发生消去反应,又能发生水解反应的是
| A.一氯甲烷 | B.1—溴—2—甲基丙烷 |
| C.1 —氯—2,2—二甲基丙烷 | D.3—氯—2,2,4,4—四甲基戊烷 |
下列离子方程式中正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++OH-+H ++SO42-= BaSO4↓+H2O ++SO42-= BaSO4↓+H2O |
B.NH4HC O3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O O3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| C.大理石溶于醋酸的反应CaCO3 + 2CH3COOH === Ca2+ + 2CH3COO-+CO2↑+ H2O |
D.FeBr2溶液中通入过量Cl2:2F e2++2Br-+2Cl2 = 2Fe3++Br2+4Cl- e2++2Br-+2Cl2 = 2Fe3++Br2+4Cl- |