化合物CO、HCOOH、HOOC—CHO(乙醛酸),分别燃烧时,消耗O2和生成CO2的体积比都是1∶2,后两者的化学式可以看成是(CO)(H2O)和(CO)2(H2O),也就是说,只要分子式符合[(CO)n(H2O)m](n和m为正整数)的各种有机物,它们燃烧时耗O2和生成CO2体积比都是1∶2。现有一些含C、H、O三种元素的有机物,它们燃烧时耗氧和生成CO2的体积比是3∶4。
(1)这些有机物中,相对分子质量最小的化合物的分子式是________。
(2)某两种碳原子数相同的有机物,若它们的相对分子质量分别是MA和MB,(MA<MB),则MB-MA必定是_________(填一个数字)的整数倍。
(3)在这些化合物中,有一种化合物,它含有两个羧基。取0.2625g此化合物,恰好能跟0.1000mol·L-1NaOH溶液25mL完全中和,由此计算得知,该化合物的相对分子质量应该是__________,并可推导出它的分子式应是____________。
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+=Fe2++H2↑。
(2)实验用品:电极________、________、稀硫酸、________(填写所缺的实验用品)、耳机(或者电流计)。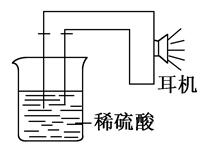
(3)实验装置:
(4)原电池设计及注意的问题。
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”声音。其原因是:在原电池中,由化学能转化为________。
②如果将装置中的耳机改为电流计,则铁钉应该接电流计的______
极,电极反应是________________;另一极应该接电流计的________极,电极发生了________反应(“氧化”或“还原”)。
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol·L-1的H2SO4溶液中,乙同学将电极放入6 mol·L-1的NaOH溶液中,如图所示。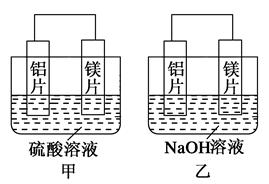
(1)写出甲中正极的电极反应式_____________________________。
(2)乙中负极为________,总反应的离子方程式:
______________________________________________________。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________活动性更强,而乙会判断出________活动性更强。(填写元素符号)
(4)由此实验得出的下列结论中,正确的有________。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,没有实用价值了 |
| D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析 |
【实验目的】利用所学知识,设计电池装置。
【实验用品】电极:镁条、铜片、铁片等。
【电解质】果汁(橙汁、苹果汁、柠檬汁等)。
【其他】导线、金属夹、发光二极管、500 mL烧杯。
【实验方案】①Cu—Mg原电池,电解质溶液为橙汁;
②Cu—Fe原电池,电解质溶液为苹果汁;
③Fe—Mg原电池,电解质溶液为柠檬汁。
【实验操作】用导线分别将三种方案中的金属片连接到金属夹上,分别将金属片两两插入到盛有果汁的三个500 mL的烧杯中,用发光二极管两端分别接触三种方案中金属活动性不同的金属夹。观察现象,连接方式如图所示。
【实验现象】三种方案中发光二极管均发光。
【实验结论】原电池把化学能转变为电能。
回答问题:
(1)连接装置时活泼金属接二极管的________极上,较不活泼金属接二极管的________极上。
(2)在方案①②中铜作电极情况__________________________。
(3)在方案①③中镁作电极情况__________________________。
(4)在方案②③中铁作电极情况__________________________。
(5)在方案③中负极反应为______,正极反应为________,总方程式为__________________________________________________________。
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上________
(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来,组成一个原电池,负极为______,正极的电极反应式为___________。
(2)如果烧杯中最初装入的是500mL 2 mol·L-1的稀硫酸,构成铜锌原电池(假设产生的气体没有损失),当在标准状况下收集到11.2 L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度应为(溶液体积变化忽略不计)________________________。
如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。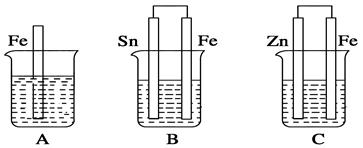
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________。
(3)C中被腐蚀的金属是________,总反应的化学方程式为_____________________。比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为__________。
(填序号)。