镁粉与碘粉均匀混合,滴加几滴水,发生剧烈反应,并产生大量紫色蒸气。以下叙述错误的是
| A.H2O作催化剂 | B.紫色蒸气是I2 |
| C.该反应是放热反应 | D.反应后物质的总能量升高 |
下列实验装置或操作正确的是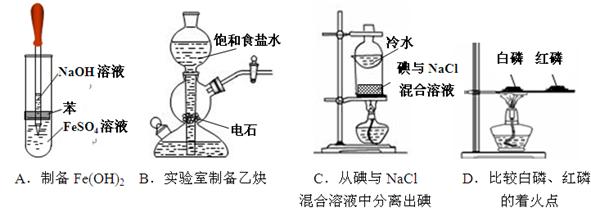
以下金属冶炼方法错误的是:
A.3MnO2 + 4Al 3Mn + 2Al2O3 3Mn + 2Al2O3 |
B.2AlCl3(熔融) 2Al + 3Cl2 2Al + 3Cl2 |
C.Fe2O3 + 3CO 2Fe + 3CO2 2Fe + 3CO2 |
D.2HgO 2Hg+ O2↑ 2Hg+ O2↑ |
以下物理量只与温度有关的是
| A.醋酸的电离度 | B.醋酸钠的水解程度 |
| C.水的离子积 | D.氨气的溶解度 |
为了确定某物质是否变质,所选试剂(括号内物质)错误的是
| A.Na2SO3是否被氧化(BaCl2) | B.FeCl2是否被氧化(KSCN) |
| C.KI是否被氧化(淀粉溶液) | D.氯水是否失效(pH试纸) |