| A.c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol/L | B.2c(CO32-)+c(HCO3-)+c(OH-)=c(Na+)+c(H+) |
| C.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | D.c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
下列物质的电子式书写正确的是
A.NaCl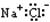 |
B.H2S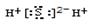 |
C.N2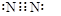 |
D.NH4I |
1919年,科学家第一次实现了人类多年的梦想——人工转变元素。这个核反应如下: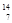 N+
N+ He→
He→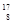 O+
O+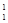 H下列叙述正确的是
H下列叙述正确的是
A.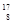 O原子核内有9个质子 O原子核内有9个质子 |
B.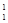 H原子核内有1个中子 H原子核内有1个中子 |
| C.O2和O3互为同位素 | D.通常情况下,He和N2化学性质都很稳定 |
下列物质中既有离子键,又有共价键的是
| A.KOH | B.CaCl2 | C.H2O | D.Cl2 |
aXn-和bYm+为两主族元素的离子,它们的电子层结构相同, 下列判断错误的是
| A.原子半径X<Y | B.a+n=b-m |
| C.Y最高价氧化物的化学式为YOm | D.X的氢化物的化学式为HnX |
元素X的原子有3个电子层,最外层有4个电子。这种元素位于周期表的
| A.第4周期ⅢA族 | B.第4周期ⅦA族 |
| C.第3周期ⅣB族 | D.第3周期ⅣA族 |