(1)2008年9月25日,“神舟七号”载人航天飞船在酒泉卫星发射中心成功发射升空。航天飞船曾用金属铝粉和高氯酸铵混合物作为固体燃料。加热铝粉使其氧化并放出大量热量,促使混合物中另一种燃料分解。m mol高氯酸铵分解时除产生2m mol水蒸气和m mol氧气外,其他组成元素均以单质形式放出,因而产生巨大的推动力。
(1)写出其中涉及的化学方程式:_____________;____________。
(2)高氯酸铵作为火箭燃料的重要供氧剂。高氯酸铵在高压、450 ℃的条件下迅速分解生成水蒸气、氮气、氯化氢和氧气。
①写出此反应的化学方程式:____________________。
②反应中生成的氧化产物与还原产物的物质的量之比是__________,每分解1 mol高氯酸铵,转移的电子数目是__________。
向橙色的溴水中通入SO2气体,观察到的现象是____________。有关的离子方程式为___________________________
在盛有淀粉碘化钾酸性溶液的试管中,滴入少量的次氯酸钠溶液后,溶液呈蓝色,说明溶液中生成了________________单质,有关的离子方程式为__________________。
磷酸(H3PO4)在水中可分三步电离,能够以H3PO4、H2PO- 4、HPO2- 4、PO3- 4等四种粒子形式存在,当溶液的pH发生变化时,其中任一粒子的物质的量占四种粒子总物质的量的分数δ(分布分数)也可能发生变化。图1是某浓度H3PO4溶液中各种粒子的物质的量分数δ随pH的变化曲线。用NaOH标准溶液滴定该H3PO4溶液,绘得滴定曲线如图2。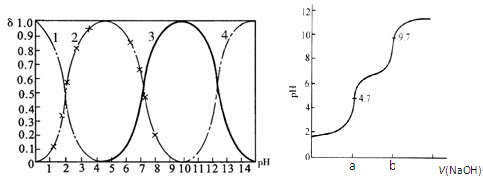
图1 H3PO4粒子分部分数与pH关系图2 H3PO4滴定曲线(部分)
(注:图中曲线1表示H3PO4、曲线2表示H2PO- 4、曲线3表示HPO2- 4、曲线4表示PO3- 4)
(1)H3PO4第一步电离的电离常数K1的表达式为_______,K1的数值最接近(填字母)______。
| A.10-2.1 | B.10-4.7 | C.10-7 | D.10-9.7 |
(2)用NaOH滴定H3PO4,写出反应从a点到b点的离子方程式____________________,当滴定至pH=7时,溶液主要存在的阴离子(OH-除外)有_______________。
(3)在Na3PO4溶液中,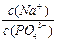 ____3(填“>”、“<”、“=”),原因是__________________(用离子方程式表示)。
____3(填“>”、“<”、“=”),原因是__________________(用离子方程式表示)。
(4)磷酸钙、磷酸一氢钙和磷酸二氢钙是三种重要的磷酸盐,在食品、化肥等方面应用广泛。其20℃时溶解度数据如下表:
| 名称 |
化学式 |
20℃时溶解度(g) |
| 磷酸钙 |
Ca3(PO4)2 |
2×10-3 |
| 磷酸一氢钙 |
CaHPO4 |
4.3×10-3 |
| 磷酸二氢钙 |
Ca(H2PO4)2 |
1.8 |
磷酸钙在水中溶解度很小,但易溶于稀盐酸。结合平衡移动原理分析其原因
_________________________________________________________________。
甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
① CH4(g)+H2O(g) 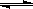 CO(g)+3H2(g)△H1
CO(g)+3H2(g)△H1
② CO(g)+2H2(g) 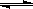 CH3OH(g)△H2
CH3OH(g)△H2
将0.20mol CH4和0.30 mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图。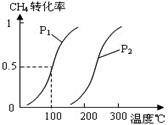
(1)已知在P1、100℃时达到平衡所需的时间为5min,则用CH4表示的平均反应速率为______。
(2)反应①的△H10,图中的P1______P2(填“<”、“=”或“>”)。
(3)在压强为0.1MPa条件下,将一定量CO与H2的混合气体在催化剂作用下能自发反应生成甲醇,则反应②的△H20,△S0(填“<”、“=”或“>”)。
(4)根据题中给出的数据,计算反应①在100℃时的平衡常数值(写出计算过程及结果)
本题包括两小题,根据你所学的内容选择(1)或(2)其中一小题回答相关问题。
(1)在A图中,请加以必要连接(在图上画上),使铜片上冒H2气泡,则连接后的装置叫,该装置实现的能量转换是________________。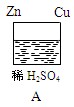
写出该装置的电极反应式:
锌片:;铜片:;
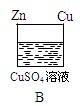
在B图中,加以必要的连接(在图上画上),使锌片上析出铜,则连接后的装置叫,
该装置实现的能量转换是________________。
写出该装置的电极反应式:
锌片: ;铜片: ;