某溶液中存在Na+、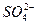 、
、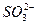 、Cl-、
、Cl-、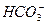 、Br-中的若干种,依次进行下列实验:
、Br-中的若干种,依次进行下列实验:
(1)用pH试纸检验,溶液的pH>7;
(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈橙色,用分液漏斗分液;
(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液,只有白色沉淀产生,过滤;
(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生。
下列判断正确的是( )
①肯定有Na+②肯定有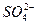 ③肯定有
③肯定有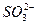
④肯定有Br-⑤肯定有Cl-⑥肯定没有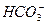
| A.①③④⑥ | B.①②④⑥ |
| C.②③④⑥ | D.③④⑤⑥ |
下列有关电化学知识的描述正确的是
| A.CaO+H2O="=" Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16 g,乙池中某电极上析出0.24 g某金属,下列说法正确的是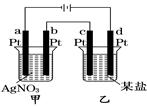
| A.甲池b极上析出金属银,乙池c极上析出某金属 |
| B.甲池a极上析出金属银,乙池d极上析出某金属 |
| C.某盐溶液可能是CuSO4溶液 |
| D.某盐溶液可能是Mg(NO3)2溶液 |
根据下图,可判断出下列离子方程式中错误的是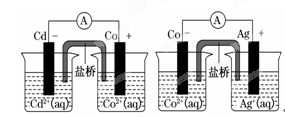
| A.2Ag(s)+Cd2+(aq)===2Ag+(aq)+Cd(s) | B.Co2+(aq)+Cd(s)===Co(s)+Cd2+(aq) |
| C.2Ag+(aq)+Cd(s)===2Ag(s)+Cd2+(aq) | D.2Ag+(aq)+Co(s)===2Ag(s)+Co2+(aq) |
常温时,以下4种溶液pH最大的是
| A.0.01 mol·L-1氨水溶液 |
| B.0.02 mol·L-1氨水与0.02 mol·L-1盐酸溶液等体积混合液 |
C.0.03 mol·L-1氨 水与0.01 mol·L-1盐酸溶液等体积混合液 水与0.01 mol·L-1盐酸溶液等体积混合液 |
| D.pH=2的盐酸与pH=12的Ba(OH)2溶液等体积混合液 |
把1 mL 0.1 mol/L的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于
| A.1×10-4 mol/L | B.1×10-8 mol/L | C.1×10-11 mol/L | D.1×10-10 mol/L |