下列有关电化学知识的描述正确的是
| A.CaO+H2O="=" Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
配制100 mL 0.10 mol·L-1的NaOH溶液时,下列实验操作会使所配溶液浓度偏大的是
| A.转移溶液时有液体飞溅 |
| B.在容量瓶中定容时俯视刻度线 |
| C.定容时凹液面最底处高于刻度线 |
| D.转移溶液后未洗涤烧杯就直接定容 |
下列实验操作或方法,不正确的是
| A.用蒸馏的方法制取蒸馏水 |
| B.用酒精萃取饱和碘水中的碘单质 |
| C.使用分液漏斗分离水和四氯化碳的混合物 |
| D.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
将饱和氯化铁溶液分别滴入下列液体中,能形成胶体的是
| A.冷水 | B.氯化钠溶液 | C.沸水 | D.氢氧化钠溶液 |
下列物质的分类合理的是
| A.氧化物:CaO、Al2O3 | B.铵盐:NH3·H2O、NH4Cl |
| C.酸:H2SO4、NaHSO4 | D.碱:NaOH、Na2CO3 |
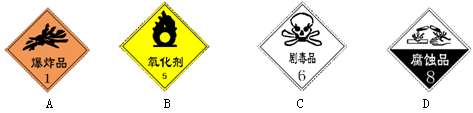
对危险化学品要在包装标签上印有警示性标志。氰化钾(KCN)应选用的标志是