体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( )
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
下表是几种电解质的电离常数(25℃) 电解质的强弱判断正确的是
电解质的强弱判断正确的是
| A.e最弱 |
| B.b最强 |
| C.由强到弱的顺序为a> b> d >e >c |
| D.无法确定 |
反应N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。正确的是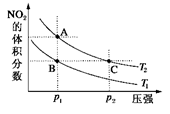
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C. A、C两点气体的平均相对分子质量:A>C
D.由状态B到状态A,可以用加热的方法
在一定温度下,向密闭容器中充入1.0molN2和3.0molH2,反应达到平衡时测得NH3的物质的量为0.6mol.若在该容器中开始时充入2.0molN2和6.0molH2,则平衡时NH3的物质的量为
| A.若为定容容器,n(NH3)="1.2mol" |
| B.若为定容容器,n(NH3)>1.2mol |
| C.若为定压容器,n(NH3)>1.2mol |
| D.若为定压容器,n(NH3)<1.2mol |
某温度下,H2(g)+CO2(g)  H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=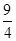 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)(mol·L-1) |
0.010 |
0.020 |
0.020 |
| c(CO2)(mol·L-1) |
0.010 |
0.010 |
0.020 |
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol·L-1
D.反应开始时,丙的反应速率最快,甲的反应速率最慢
常温下,1 mol化学键分解成气态原子所需要的能量用E表示。结合下表信息判断不正确的是
| 共价键 |
H-H |
F-F |
H-F |
H-Cl |
H-I |
| E(kJ·mol -1 ) |
436 |
157 |
568 |
432 |
298 |
A.H2(g)+F2(g)=2HF(g) △H=—25 kJ·mol -1
B.表中最稳定的共价键是H—F键
C.H 2(g)→2H(g) △H=+436 kJ·mol -1
D.432 kJ·mol -1>E(H-Br)>298 kJ·mol -1