50 g镁、锌、铝的混合物与适量的稀硫酸反应,得三种盐的混合溶液,然后加热、蒸发、结晶得晶体(不含结晶水)218 g,则反应中得H2的质量为( )
| A.2 g | B.3 g |
| C.3.5 g | D.4.5 g |
下列过程不能实现化学能转化为热能的是()
| A.二氧化硫催化氧化生成三氧化硫 | B.电解氯化钠水溶液 |
| C.铝粉与四氧化三铁反应 | D.铁与盐酸反应 |
绿色化学的核心是提高原子的利用率,最理想的“原子经济”是指原子利用率为100% 。下列有机反应中,原子利用率最高的反应是()
A.CH4+Cl2 CH3Cl+HCl CH3Cl+HCl |
B.nCH2=CH2 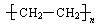 |
C. +HO—NO2 +HO—NO2  +H2O +H2O |
D.2CH3CH2OH+O2 2CH3CHO+2H2O 2CH3CHO+2H2O |
用NA表示阿伏加德罗常数的值。下列判断正确的是()
| A.常温常压下,18 g2H2O含有的原子总数目为3NA |
| B.常温常压下,22.4 L Cl2中含有的分子数为NA |
| C.1 mol Na在O2中完全燃烧转移的电子数目为NA |
| D.1 mol·L-1 KHSO4溶液中含有的钾离子数目为NA |
下列实验方法或操作能达到实验目的的是()
| A.图1:石油分馏 |
| B.图2:配制150 mL 0.1 mol/L盐酸 |
| C.图3:烧瓶内溶液变蓝色 |
| D.图4:探究NaHCO3的热稳定性 |
一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2 + 3H2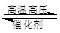 2NH3(正反应是放热反应)。下列有关说法正确的是()
2NH3(正反应是放热反应)。下列有关说法正确的是()
| A.降低温度可以加快反应速率 |
| B.达到化学反应限度时,生成2mol NH3 |
| C.向容器中再加入N2可以加快反应速率 |
| D.1mol N2和3mol H2的总能量低于2mol NH3的总能量 |