可以从以下角度判断氯元素和硫元素非金属性的强弱:
(1)在元素周期表中,氯元素和硫元素的相对位置是__________________________,根据____________________________规律来判断氯元素和硫元素非金属性的强弱。
(2)二者气态氢化物中______________(填化学式)更易分解,由此可判断氯元素和硫元素非金属性的强弱。
(3)向硫化氢溶液中通入氯气,溶液变浑浊,反应的化学方程式为__________________,说明氯元素的非金属性比硫元素________________(填“强”或“弱”)。
(4)氯气和硫分别与铁形成化合物的化学式为________________和________________,据此也可判断氯元素和硫元素非金属性的强弱。
(一)写出下列有机物的系统命名或结构简式:
(1)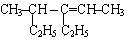 _____________________________
_____________________________
(2)CH3CH(CH3)C(CH3)2(CH2)2CH3
(3) 2-甲基-2-戊烯 _____________________________________
(二).下面列出了几组物质,请将物质的合适组号填写在下表中。
① 和
和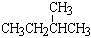 ; ②
; ② 和
和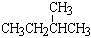 ;
;
③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦35Cl2和37Cl2
⑧乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑨氧气(O2)与臭氧(O3)⑩ H2O与D2O
| 类别 |
同位素 |
同系物 |
同素异形体 |
同分异构体 |
| 组号 |
Ⅰ 浓度为0.1 mol·L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+)依次为a mol·L-1,b mol·L-1,c mol·L-1,其由大到小的顺序是________。
(2)完全中和一定量NaOH溶液时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为__________________________________。
(3)与锌反应开始时产生氢气的速率分别为v1、v2、v3,其由大到小的顺序是________。
Ⅱ c(H+)相同的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液均加水稀释至体积为原来的10倍, c(H+)依次为a mol·L-1,b mol·L-1,c mol·L-1,其由大到小的顺序是_______。
(2)三种溶液体积相同时,同时加入相同的锌,若产生相同物质的量的氢气,所需时间分别为t1、t2、t3,其大小关系是___________.
(1)某温度(T℃)时,测得0.01 mol/L NaOH溶液的pH为11,则该温度下水的KW=________。则该温度________(填“大于”、“小于”或“等于”)25℃,其理由是___________________________________________________。
(2)此温度下,将pH=a的NaOH溶液Va L与pH=b的HCl溶液Vb L混合,若所得混合溶液为中性,且a=12,b=2,则Va∶Vb=________。
下面所列物质中,属于电解质的是__________(填序号,下同),属于非电解质的是________,属于强电解质的是__________,属于弱电解质的是________。
①CH3CH2OH ②CH3COOH ③熔融态KNO3 ④SO3 ⑤蔗糖 ⑥HF ⑦NaHCO3 ⑧氨水 ⑨Cl2 ⑩BaSO4 ⑪Cu
下表列出了①~⑥六中元素在周期表中的位置:
族 周期 周期 |
ⅠA |
0 |
||||||
| 1 |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
||
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
请按要求回答下列问题:
(1)写出下列标号元素的元素符号:①、⑤ 。
(2)④和⑥两种元素形成的化合物的电子式是。
(3)元素②形成的最简单有机物的空间结构为。
(4)元素④的单质在氧气中燃烧的化学方程式是。