碘缺乏症遍及全球,多发生于山区。南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区。我国云南、河南等10余省的山区发病率也较高。据估计我国患者大约有1000万人。为控制该病的发生,较为有效的方法是食用含碘食盐,我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3)。据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一
A.胰岛素 B.甲状腺激素 C.生长激素 D.雄性激素
(2)长期生活在缺碘山区,又得不到碘盐的供应,易患
A.甲状腺亢进 B.佝偻病 C.地方性甲状腺肿 D.糖尿病
(3)可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾。反应的化学方程式为 。氧化产物与还原产物的物质的量之比为 。能观察到的明显现象是 。
(4)已知KIO3可用电解方法制得。总反应化学方程式为:KI+3H2O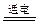 KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。
KIO3+3H2↑。在某温度下.若以12 A的电流强度电解KI溶液10 min.理论上可得标况下氢气___________L。
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号______________;D的原子结构示意图______________。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是_______________________。
(3)A、B、C、D形成的化合物B2A2、CD2、D2A、DA2中各原子都满足最外层8电子结构的是______________(填写具体的化学式 )。
(4)CA2与D元素的单质在水溶液中反应的化学方程式是______________________________。
已知A元素核外K、L电子层的电子总数与M、N电子层的电子总数相等,B元素的一种单质是自然界中硬度最大的物质。回答下列问题:
(1)A的元素符号为_________,B的元素符号为_________。
(2)在电弧作用下,A的氧化物能与B的单质反应,生成AB2和一种能与人体的血红蛋白结合的气体。写出AB2与水反应生成气体C的化学方程式:_____________________________。
(4分)A、B、C、D、E、F六种短周期元素的原子序数依次增大。已知A、C、F三原子的最外层共有11个电子,且这三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4,E元素原子的次外层电子数比最外层电子数多3。试回答:
(1)写出下列元素的符号:A_________,D_________,E_________。
(2)用电子式表示B、F形成化合物的过程:__________________________________________。
(3)A、C两种元素最高价氧化物的水化物反应的离子方程式:_________________________。
(4)D的固态氧化物是__________晶体,含n mol D的氧化物的晶体中含D—O共价键为____________mol。
下图表示一些晶体中的某些结构,它们是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分。
(1)其中代表金刚石的是____________(填编号字母)。晶体中每个碳原子与____________个碳原子最接近且距离相等。金刚石属于____________晶体。
(2)其中代表石墨的是________。晶体中每个正六边形占有的碳原子数平均为_________个。
(3)其中表示NaCl的是____________。
(4)其中表示CsCl的是____________,CsCl属于____________晶体。
(5)其中表示干冰的是____________,干冰属于____________晶体。晶体中每个CO2分子与____________个CO2分子距离相等,且最接近。
(6)上述五种物质按熔点由高到低的排列顺序为__________________________________。
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。
已知:
①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是 。
(2)Z2Y2与X2Y反应的化学方程式是 。
(3)如图4-22所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。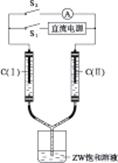
图4-22
接通S1,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:
C(Ⅰ)的电极名称是 (填“正极”或“负极”);
C(Ⅱ)的电极反应式是 。
(4)铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是。