工业利用上述信息,按图所示的路线合成物质M(结构简式如右图所示),该物质是一种香料。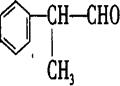
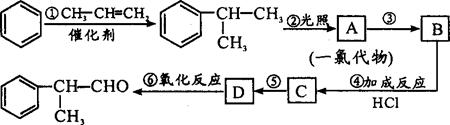
请根据上述路线,回答下列问题:
(1) A的结构简式可能为:(只写一种) 。
(2) M中含氧官能团的名称是 。
(3) 写出反应④的化学方程式为(有机物写结构简式,并注明反应条件):
_______________________________________________ _______。
(4) 写出D和浓硫酸共热发生消去反应的化学方程式
(5)这种香料具有多种同分异构体,写出其中一种能同时满足下列条件的同分异构体结构简式_________________________________。
a.该物质的水溶液遇FeCl3溶液呈紫色;
b.分子中有苯环,且苯环上的一溴代物有两种。
质量为34 g的NH3其物质的量是mol,在标准状况下的体积约为L 。0.1 mol H2S中有约个氢原子;相同质量的NH3和H2S中分子个数比为。配制100 mL浓度为1 mol·L-1的稀硫酸,需要用98%密度为1.84 g/cm3的浓硫酸mL。
(6分)根据题目要求书写化学用语:
(1)碳酸氢钠的电离方程式。
(2) 钠和水反应的离子方程式。
(3) 符合CO2+2OH—===CO32-+H2O的化学方程式。
某条件下,在2L密闭容器中发生如下反应:2NO2(g) 2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。
2NO(g)+O2(g) △H>0。在三种不同条件下进行,其中NO、O2的起始浓度都为0 mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。
请回答下列问题:
(1)请在图中标上对应的反应温度(800℃或850℃)。实验Ⅱ隐含的反应条件是_______________________。
(2)写出该反应的平衡常数表达式:K=______________。
(3)若实验Ⅰ中达平衡后,再向密闭容器中通入1mol NO2与1mol NO混合气体(保持温度不变),则平衡将_________(填“正向移动”或“逆向移动”或“不移动”)
(4)一定条件下NO2与SO2可发生反应,其方程式为:
NO2(g)+SO2(g) SO3(g)+NO(g) △H>0,将NO2与SO2以体积比
SO3(g)+NO(g) △H>0,将NO2与SO2以体积比 置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
A、体系压强保持不变 B、混合气体颜色保持不变
C、SO3和NO的体积比保持不变 D、混合气体的平均相对分子质量保持不变
(5)若改变条件,使平衡常数变大,该反应 。
A、一定向正反应方向移动 B、在平衡移动时,正反应速率先增大后减小
C、一定向逆反应方向移动 D、在平衡移动时,逆反应速率先增大后减小
2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是。
(2)在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中,①NH4+、Al3+、Br-、SO42-
② Na+、Mg2+、Cl-、NO3-③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-四组离子中,一定可以大量共存的是(填序号,下同),可能大量共存的是。
(3)在下列反应中,水仅做氧化剂的是(填字母,下同),水既不做氧化剂又不做还原剂的是。
| A.Cl2+H2O=HCl+HClO |
| B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.CaH2+2H2O=Ca(OH)2+2H2↑ |
D.3Fe+4H2O Fe3O4+4H2 Fe3O4+4H2 |
(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为。
(5)右图是某品牌饮用矿泉水标签的部分内容。请认真阅读标签内容后计算。
①该矿泉水中镁离子的物质的量浓度的最大值是;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过mol。
W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为。
(2)W与Y可形成化合物W2Y,该化合物的电子式为。
(3)X的硝酸盐水溶液显性,用离子方程式解释原因:。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为。
(5)比较Y、Z气态氢化物的稳定性:>(用分子式表示)。
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是>>>。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:。