下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融)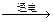 2Na+Cl2 2Na+Cl2 |
B.MgO+H2 Mg+2H2O Mg+2H2O |
C.Fe3O4+CO  3Fe+4CO 3Fe+4CO |
D.2HgO  2Hg+O2 2Hg+O2 |
几种短周期元素的原子半径及主要化合价如下表
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是
| A.X、Y元素的金属性 X<Y |
| B.一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C.Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D.一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
短周期元素X.Y.Z所在的周期数依次增大,它们的原子序数之和为20,且Y2—与Z+核外电子层的结构相同。下列化合物中同时存在极性和非极性共价键的是
| A.Z2Y | B.X2Y2 | C.Z2Y2 | D.ZYX |
NA为阿伏加德罗常数,下列说法错误的是
| A.0.1mol的甲基(—CH3)与羟基(—OH)所含电子数均为NA |
B.1molD216O中含中子、质子、电子各10NA |
| C.32 g S8单质(分子结构如图)中含有的S—S键个数为NA |
| D.1.5g CH3+中含有的电子数为0.8NA |
已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论错误的是
| A.氯化铝是电解质 | B.固体氯化铝是分子晶体 |
| C.可用电解熔融氯化铝的办法制取金属铝 | D.氯化铝为非极性分子 |
在乙烯分子中有5个σ键、一个π键,它们分别是
| A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 |
| C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 |
| D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键 |