把河沙(主要成分是SiO2)跟镁粉按一定质量比(质量比约大于15∶24)混合均匀,装入试管中加热大约一分钟后发生剧烈反应,生成一种白色固体化合物和一种硅化物.待生成的混合物冷却后放入盛有稀硫酸的烧杯中,立即产生气泡并伴有爆炸声,产生的气体是一种能在空气中自燃的气态氢化物.
(1)写出河沙与镁粉在加热条件下的化学方程式: ,该反应是__________(填“放热”或“吸热”);
(2)生成的混合物放入稀硫酸中,产生的气体是(填分子式)__________;
(3)写出产生“爆炸声”的化学方程式: 。

已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化 物A起反应。
物A起反应。
据此,请填空:
⑴化合物F的化学式为__________,化合物I的化学式为_____________,氧化物A的晶体类型为_____________。
⑵反应①的化学方程式为___________________________________。
⑶氧化物A与烧碱溶液反应的离子方程式为___________________________________。
三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要 求回答下列问题:
求回答下列问题:
⑴写出制备NF3的化学反应方程式:。反应过程中,氧化剂与还原剂的物质的量之比为。
⑵写出三氟化氮与水蒸气反应的化学方程式:。⑶NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体
泄漏时的现象是。
⑷一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种
钠盐:(填化学式)。
⑴24 mL 0.05 mol·L-1的Na2SO3溶液恰好被20 mL 0.02 mol·L-1的K2R2O7溶液氧化,则元素R在还原产物中的化合价是________。
⑵将0.64 g Cu全部溶于一定量的浓硝酸中,测得生成气体0.009 mol(含NO、NO2和N2O4),共消耗硝酸0.032 mol。将生成的气体与空气混合,再通入NaOH溶液中,氮氧化物被完全吸收,产物只有NaNO3和H2O。计算空气中参加反应的O2在标准状况下的体积 为________mL。
为________mL。
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 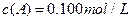 、
、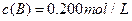 及
及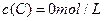 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。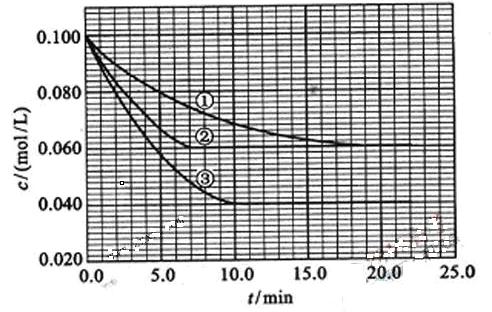
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
② ;
③
(2)实验②平衡时B的转化率为 _________;实验③平衡时C的浓度为____________;
(3)该反应的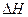 ____
____ _____0,判断其理由是_____________________;
_____0,判断其理由是_____________________;
(4)该反应进行到4.0min时的平均反应速率:
实验②: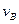 =;
=;
实验③: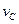 =____________________。
=____________________。
反应m A+n B p C在某温度下达到平衡。
p C在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是
______ _________。
②若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向______方向移动。
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为_____态。