向含有等物质的量的NaCl和NaBr的混合溶液中通入足量的氯气,反应完全后,将溶液蒸发至干,可得固体物质58.5 g,则原混合溶液中含Na+_______mol,含NaBr________g。
天然维生素P(结构如下图,分子结构中R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述正确的是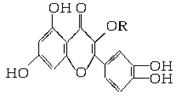
| A.可与溴水反应,且1 mol该物质与足量溴水反应消耗6 mol Br2 |
| B.可与NaOH溶液反应,1 mol该物质可与5 mol NaOH反应 |
| C.一定条件下1 mol该物质可与H2加成,耗H2最大量为6 mol |
| D.维生素P能发生水解反应 |
孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:
x CuCO3 •y Cu(OH)2(x、y为正整数且x≤2,y≤2)。
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4︰1;石青则为3︰1。请推算它们的化学组成(化学式)。
孔雀石:;石青:。
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 4.48L(标准状况下);加热另一份样品使其完全分解,得到CuO28g,试通过计算确定该混合物中孔雀石和石青的物质的量之比为。
(12分)某化学兴趣小组用只含有铝、铁、铜的工业废料制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
(1)写出合金与烧碱溶液反应的离子方程式: 。
(2)由滤液A制AlCl3溶液的途径有①和②两种,你认为较合理的途径及理由是: 。
(3)滤液E若放置在空气中一段时间后,溶液中的阳离子除了 和
和 外,还可能存在 (用元素符号表示)。
外,还可能存在 (用元素符号表示)。
(4)用滤渣F通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是:
、 。
(5)途径④发生反应的化学方程式为: 。
(6)实验室从CuSO4溶液制取胆矾,操作步骤有蒸发浓缩、冷却结晶、 、自然干燥。
(8分)有机物A、B、C、D有如下性质。
(1)具有支链的化合物A的分子式为C4H6O2,A可以使Br2的四氯化碳溶液褪色。1molA
和1mol NaHCO3能完全反应,则A的结构简式是。
写出与A具有相同官能团的A的所有同分异构体的结构简式
。
(2)化合物B含有C、H、O三种元素,分子量为60,其中碳的质量分数为60%,氢的质量分数为13.33%。B在催化剂Cu的作用下被氧化成C,C能发生银镜反应,则B的结构简式是。
(3)D在NaOH水溶液中加热反应,可生成A的钠盐和B,相应反应的化学方程式是
。
A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去)。
试回答:
(1)若X是强氧化性单质,则A不可能是。
a. S b. N2 c. Na d. Mg e. Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属元素价态的操作方法是:。则B的化学式为。
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,B为两性化合物,则X的化学式可能为(写出不同类物质)或,
反应①的离子方程式为(写一条)。