为了使0.1 mol·L-1 Na2CO3溶液中c(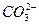 )接近0.1 mol·L-1,应采取( )
)接近0.1 mol·L-1,应采取( )
| A.加水 | B.通入CO2 |
| C.加入少量盐酸 | D.加入少量固体NaOH |
据报道,科学家最近发现了一种新的粒子,这种粒子是由3个1 H原子核和2个电子构成。下列关于这种粒子的说法中,正确的是
| A.它是氢的一种新同位素 | B.这种新元素的核电荷数是3 |
| C.它是H2的一种新同素异形体 | D.它比一个普通氢分子多—个氢核 |
下列各对物质间的反应既属于氧化还原反应,又属于离子反应的是
| A.Zn+H2SO4(稀) | B.NaCl+AgNO3(溶液) |
| C.H2+O2 | D.Na2O+H2O |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是
A.次氯酸的电子式: |
B.质量数为16的氧原子: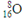 |
C.乙烯的结构简式: |
D.碳酸氢根离子的电离方程式: HCO3-+ H2O H3O++ CO32- H3O++ CO32- |
下列实验能达到预期目的的是
| A.通过电泳实验证明胶体带电 |
| B.通常利用丁达尔效应区别溶液与胶体 |
| C.渗析实验说明胶体粒子能透过半透膜 |
| D.向煮沸的NaOH溶液中滴加FeCl3溶液可制备Fe(OH)3胶体 |
判断下列有关化学基本概念的依据正确的是
| A.氧化还原反应:元素化合价是否变化 | B.共价化合物:是否含有共价键 |
| C.强弱电解质:溶液的导电能力大小 | D.氧化物:含氧化合物 |