已知某溶液中只存在OH-、H+、 和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c( )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
②c(Cl-)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c( )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c( )>c(OH-)
)>c(OH-)
填写下列空白。
(1)若溶液中只溶解了一种溶质,则该溶质是____________,上述四种离子浓度的大小顺序为_________________(填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为____________,若上述关系中④是正确的,则溶液中的溶质为____________________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_________c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)与碱中c(OH-)的关系是__________________。
已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题: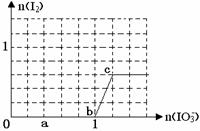
(1)写出a点反应的离子方程式;
反应中还原剂是;被还原的元素是。
(2)写出b点到c点反应的离子方程式。
(3) 当溶液中的I-为0.4 mol时,加入的KIO3为mol。
当溶液中的I-为0.4 mol时,加入的KIO3为mol。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
。
下表为元素周期表短周期的一部分。回答下列问题:
| A |
D |
|||
| E |
G |
M |
(1)E元素原子核外有2个未成对电子,这2个电子所处亚层的符号是;请从物质的类别、化合价二方面归纳该元素+4价氧化物的化学性质:。
(2)请指出G的非金属性比E的非金属性强的事实(写3)。 (3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释。
(3)E、G元素的原子均可形成与M原子电子层结构相同的简单离子,且E离子的半径更大,请解释。
(4)A与氢元素形成分子的空间结构可能是(选填序号)。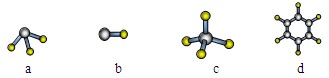
有浓度为0.1 mol•L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol·L-1,b mol·L-1,c mol·L-1,其大小顺序为__________。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为
n 1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为____________。
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其大小关系为____________。
若以铁棒、碳棒、导线和氯化铁溶液为用品设计原电池。电池反应式为_________________________。
某温度(t℃)时,水的KW=10-13则该温度(填大于、等于或小于)______25℃,理由是________________________________________________