
其中,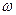 (W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是( )
(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是( )
| A.图I可能是不同压强对反应的影响,且P2>P1,a+b<n |
B.图III可能是不同温度对反应的影响,且T1>T2,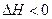 |
| C.图II可能是不同压强对反应的影响,且P1>P2,n<a+b |
| D.图II可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好 |
恒温下,下列物质的状态变化中,△S变化最大的是()
| A.H2O(l)=H2O(g) | B.H2O(s)=H2O(g) |
| C.H2O(s)=H2O(l) | D.H2O(l)=H2O(s) |
在一固定容积的密闭容器中充入2 mol A 和1 mol B ,发生反应:2A(g)+ B(g) xC(g),达到平衡后,C的体积分数为W% 。若维持容器体积和温度不变,按0.6 mol A、0.3 mol B、1.4 mol C 为起始物质,达到平衡后,C的体积分数也为W% ,则x值为()
xC(g),达到平衡后,C的体积分数为W% 。若维持容器体积和温度不变,按0.6 mol A、0.3 mol B、1.4 mol C 为起始物质,达到平衡后,C的体积分数也为W% ,则x值为()
A.只能为2 B.只能为3 C.可能是2,也可能是3 D.无法确定
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是()
2Z(g)一定达到化学平衡状态的是()
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
某温度下,在密闭容器中进行SO2的催化氧化反应。若起始时[SO2]=[O2]=6mol/L,平衡时测得[O2]=4.5mol/L,则下列叙述中正确的是()
| A.SO2的转化率为60% |
| B.SO3的产率为50% |
| C.平衡时总压强与起始压强之比为7∶8 |
| D.平衡时VSO2∶VO2∶VSO3=3∶3∶1 |
可逆反应mA(s)+nB(g) cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如下图所示(T2>T1),下列叙述错误的是()
cC(g)+fD(g)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如下图所示(T2>T1),下列叙述错误的是()
| A.达到平衡后,若使用催化剂,C的体积分数增大 |
| B.达到平衡后,若使温度升高,化学平衡向逆反应方向移动 |
| C.化学方程式中n<c+f |
| D.达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 |