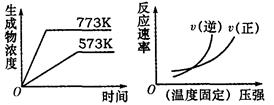
A.N2(g) +3H2(g) 2NH3(g)△H=—Q1kJ·mol—1(Q1>0) 2NH3(g)△H=—Q1kJ·mol—1(Q1>0) |
B.2SO3(g) 2SO2(g)+O2(g)△H=+Q2kJ·mol—1(Q2>0) 2SO2(g)+O2(g)△H=+Q2kJ·mol—1(Q2>0) |
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-Q3kJ·mol—1(Q3>0) 4NO(g)+6H2O(g)△H=-Q3kJ·mol—1(Q3>0) |
D.H2(g) +CO(g) C(s)+H2O(g)△H=+Q4kJ·mol—1(Q4>0) C(s)+H2O(g)△H=+Q4kJ·mol—1(Q4>0) |
高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O===3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述正确的是
| A.放电时,负极反应式为3Zn-6e-+6OH-===3Zn(OH)2 |
| B.放电时,正极区溶液的pH减小 |
| C.充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 |
| D.充电时,电池的锌电极接电源的正极 |
将含有0.4molCuSO4和0.2molNaCl水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3molCu,另一电极上析出气体在标况下的体积为
| A.4.48L | B.5.6L | C.6.72L | D.13.44L |
下列溶液一定呈中性的是
| A.c(H+)=c(OH-)=10-6 mol·L-1的溶液 |
| B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.酸与碱恰好完全反应生成正盐的溶液 |
下列表述正确的是
| A.0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| B.0.1mol·L-1CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) |
| C.CH3COONa、NaOH和Na2CO3三种溶液的pH相同,则浓度大小顺序:c (NaOH)<c(Na2CO3)<c(CH3COONa) |
| D.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,离子浓度的关系:c(CH3COO-)>c(Na+)>c(OH-)=c(H+) |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
| B.反应开始时10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始时10s,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |